
题目列表(包括答案和解析)
2.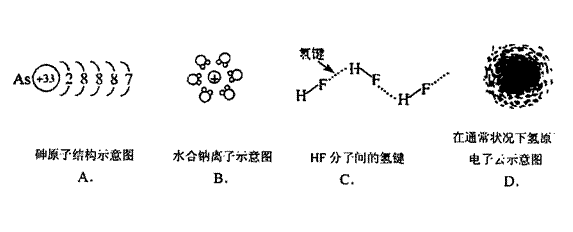 用示意图或图示的方法能够直观形象地将化学知识传授给学生,下列示意图或图示确的是 ( )
用示意图或图示的方法能够直观形象地将化学知识传授给学生,下列示意图或图示确的是 ( )
1.化学与科技、社会、生产有密切联系,下列说法正确的是 ( )
A.氮化硅陶瓷、光导纤维均属于新型有机高分子材料
B.用有机分子和C60制成“纳米车”,说明人类操纵分了技术已进入新阶段
C.建筑材制ETFE为四氟乙烯与乙烯反应的共聚物,因此ETFE为纯净物
D.光化学烟雾的产生与氮氧化物无关,因此氮氧化物可以任意排放
22.(11分)将51.2gCu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合气体共A mol,将这些气体通入适量烧碱溶液,气体全部被吸收,共消耗NaOH B mol。
(1)此过程涉及有关反应的方程式:
①N2O4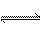 2NO2;
2NO2;
②NO+NO2+2NaOH 2NaNO2+H2O
写出③NO2被NaOH吸收的化学反应方程式 ;
(2)若A=0.8,B=1.0时,原混合气恰好被吸收,则0.8mol混合气体中NO的物质的量为 、N2O4的物质的量为 、NO2的物质的量为 ;
(3)求A=0.8时,气体与碱恰好完全反应所得溶液中NaNO3的物质的量为
(用含B的代数式表示)。(写出解题过程)
豫南七校2008-2009学年度上期期末联考
21.(8分)下图甲是课本中验证铜和浓硝酸反应的装置,乙、丙是师生对演示实验改进后的装置:
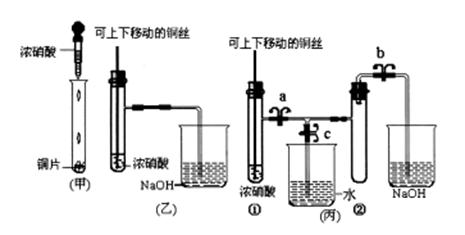
(1)甲、乙、丙三个装置中共同发生的离子反应方程式是 。
(2)和甲装置相比,乙装置的优点是① ② 。
(3)当气体充满②试管后,将铜丝提起与溶液脱离,欲使烧杯中的水进入②试管应如何操作 ______________________________________________________ 。
(4)当②试管中的NO2和水充分反应,所得溶液物质的量浓度的最大值是 。(不考虑NO2与N2O4的转化且该实验条件下气体摩尔体积设为Vm L/mol)
20.(12分)常温下有浓度均为0.5mo1/L的四种溶液:
①Na2CO3; ②NaHCO3 ③HC1 ④NH3·H2O
(1)上述溶液中,可发生水解的是 (填序号,下同)。
(2)上述溶液中,既能与氢氧化钠反应,又能和硫酸反应的溶液为 。
(3)向溶液④中加入少量氯化铵固体,此时c(NH4+)/c(OH-)的值 (填增大、减小、不变)。
(4)若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积 ④的体积(填大于、小于、等于),此时溶液中离子浓度由大到小的顺序是 。
(5)取10mL溶液③,加水稀释到500mL。,则该溶液中由水电离出的c(H+)= 。
19、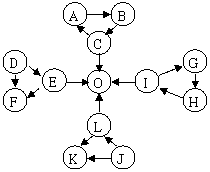 (10分)某校科研小组在探究常见物质转化时,发现部分物质可以存在如下图所示的三角关系
(10分)某校科研小组在探究常见物质转化时,发现部分物质可以存在如下图所示的三角关系
已知:
图中每个小三角形的三种物质中至少含有
一种相同元素。
②D、J为固体单质,O为气体单质,其余物质为常见化合物。
③A能使品红溶液褪色,也能使澄清的石灰水变浑浊;E为淡黄色化合物,与C反应生成O;与L反应也能生成O;K、L含有完全相同的元素。
④I为氧化物,电解可生成O,G和L反应生成难溶物H,H具有较强的吸附性。
(1)F的电子式为 。E物质中所含化学键类型有
(2)写出L→J的化学方程式 。
(3)常温下,测得一定浓度G溶液的pH==10,试用离子方程式表示其原因:
。
(4)写出E和C反应的离子方程式 。
17.对于可逆反应N2(g)+3H2(g)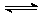 2NH3(g);△H<0,下列研究目的和示意图相符的是( )
2NH3(g);△H<0,下列研究目的和示意图相符的是( )
|
|
A |
B |
C |
D |
|
研究目的 |
压强对反应的影响(P2>P1) |
温度对反应的影响 |
平衡体系增加N2对反应的影响 |
催化剂对反应的影响 |
|
图示 |
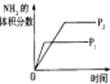 |
 |
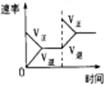 |
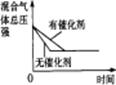 |
豫南七校2008-2009学年度上期期末联考
|
座号 |
|
高三化学试卷
得分栏
第I卷答题栏
第II卷(非选择题 共49分)
16.混合下列各组物质使之充分反应,加热蒸干产物并在300℃灼烧至质量不变,最终残留固体为纯净物的是( )
A.向CuSO4溶液中加入一小块金属钠
B.等物质的量浓度、等体积的(NH4)2SO4与BaC12溶液
C.等物质的量的NaHCO3与Na2O2固体
D.在NaBr溶液中通入少量氯气
15.下图两个装置中,液体体积均为200 mL,开始工作前电解质溶液的浓度均为0.5 mol/L,工作一段时间后,测得有0.02 mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )
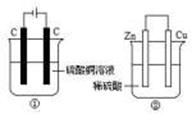 A.产生气体体积 ①=②
A.产生气体体积 ①=②
B.①中阴极质量增加,②中正极质量减小
C.电极反应式:
①中阳极:4OH- - 4e- = 2H2O+O2↑ ②中负极:2H++2e-=H2↑
D.溶液的pH变化:①减小,②增大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com