
题目列表(包括答案和解析)
20.(16分)某有机物A(只含C、H、O)是一种重要化工生产的中间体,其蒸气密度是相同状况下氢气密度的83倍。试根据下列信息回答相关问题:
①A分子中碳原子总数是氧原子总数的3倍,其苯环上只有一个取代基,且取代基碳链
上无支链;
②A可与NaHCO3溶液作用,产生无色气泡;
③A在一定条件下可与乙酸发生酯化反应。
(1)请写出:A的分子式____________;A的一种可能的结构简式____________;
A中含氧官能团的名称___________________。
若有机物A存在如下转化关系(见下框图),请据此时A的结构回答(2)、(3)、(4)小题:
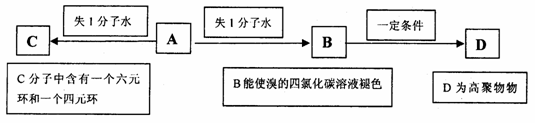
(2)请写出:A→C和B→D的化学反应方程式(注明反应条件),并注明反应类型:
A→C:________________________,反应类型:____________;
B→D:________________________,反应类型:____________。
(3)A的一种同分异构体F,其苯环上有两个相邻的取代基,且能与三氯化铁溶液发生显色反应。F在稀硫酸存在下水解生成G和H,其中H俗称“木精”,是饮用假酒过程中致人失明、甚至死亡的元凶。
请写出F的结构简式:____________________。
(4)已知H在一定条件下可被氧化成K,K的水溶液常用作防腐剂,请写出:H→K的化
学方程式:__________________________________。

19.(10分)短周期常见元素形成的纯净物A、B、C、D、E转化关系如下图所示,物质A与物质B之间的反应不在溶液中进行(E可能与A、B两种物质中的某种相同)。
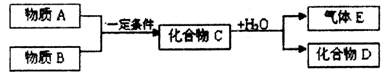
请回答下列问题:
(1)若C是离子化合物,D是一种强碱,写出C的化学式____________。
(2)若C发生水解反应,E的水溶液呈现弱酸性,D是既能溶于强酸、又能溶于强碱的
化合物。
①用电离方程式解释D既能溶于强酸,又能溶于强碱的原因(仅写出电离方程式即可)。
___________________________________________________________。
②用等式表示E与NaOH反应生成的正盐溶液中所有离子浓度之间的关系为
_________________________________________________________。
 (3)若C是一种气体,D是一种强酸,则:
(3)若C是一种气体,D是一种强酸,则:
①C与水反应的化学方程式为________________。
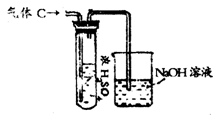
②有人认为“浓H2SO4可以干燥气体C”。某同学
为了验证该观点是否正确,用右图装置进行实验。
实验过程中,浓H2SO4中未发现有气体逸出,且变
为红棕色,则你得出的结论是______________。
18.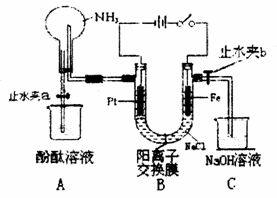 (10分)某课外活动小组设计了如图所示的装置,用于进行缓慢电解NaCl溶液及相关实验(此时打开止水夹a,关闭止水夹b)。由于某些原因,实验开始并没有达到预期的目的,但也看到了令人高兴的现象(阳离子交换膜只允许阳离子和水的通过)。请帮他们分析原因,然后回答问题:
(10分)某课外活动小组设计了如图所示的装置,用于进行缓慢电解NaCl溶液及相关实验(此时打开止水夹a,关闭止水夹b)。由于某些原因,实验开始并没有达到预期的目的,但也看到了令人高兴的现象(阳离子交换膜只允许阳离子和水的通过)。请帮他们分析原因,然后回答问题:
(1)写出B装置中的电极反应:
阴极:___________________________
阳极:___________________________
(2)一段时间内依次观察到A中的现象为:
①______________________________________
②______________________________________
③______________________________________
(3)当观察完A中的现象后,打开止水夹b。再观察C装置,若无现象说明理由,若有
现象请写出有关反应的化学方程式。_____________________________________。
(4)着想达到电解NaCl溶液的目的,请对该装置进行最简单的改进______________。
17.(9分)现有A、B、C、D、E、F六种短周期元素,原子序数依次增大。已知A与D、C与E分别同主族,D、E、F同周期.A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C形成电子总数相等的分子,且A与C形成的化合物常温下均为液态,A分别与E、F形成电子总数相等的气体分子。
请回答下列问题:
(1)元素F在周期表中的位置_______________;
(2)A、C、D三种元素可组成一种常见化合物,该化合物的化学式________________;
生产该化合物和单质F的工业称为____________工业;
(3)B与F形成的化合物分子中,各原子均达8电子结构,则该分子的电子式为
_________________________;
(4)已知0.5molEC2被C2氧化成气态EC3,放出49.15kJ热量,其热化学方程式为_____________________________________________________________;
(5)A、B、C以原子个数比4∶2∶3所形成的化合物,晶体类型为_________。
16.(10分)
(1)配平氧化还原反应方程式:
_____C2O42-+______MnO4-+______H+=_______CO2+_______Mn2++______H2O
(2)称取6.0g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250mL溶
液。量取两份此溶液各25mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25mol/LNaOH溶液至20mL时,溶液由无色变
为浅红色。该溶液被中和的H+的物质的量为________mol。
②第二份溶液中滴加0.10mol/L的酸性高锰酸钾溶液至16mL时反应完全,此时溶液
颜色由_______变为________。该溶液中还原剂的物质的量为_______mol。
⑧原试样中H2C2O4·2H2O的质量分数为__________。
15.将-定量的钠铝合金置于水中,合金全部溶解,得到20mL
pH=14的溶液,然后用1mol·L-1的盐酸滴定,至沉淀质量
最大时,消耗盐酸40mL,原合金中钠的质量为( )
A.0.46g B.0.69g C.0.92g D.0.23g
第Ⅱ卷(非选择题,共55分)
14.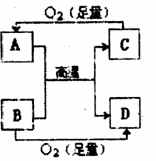 右图所示的反应均是在高温或引燃后进行。选项中的物质表
右图所示的反应均是在高温或引燃后进行。选项中的物质表
示A和B,不合理的是( )
A.CO2、Mg
B.MgO、Al
C.Fe3O4、Al
D.CuO、H2
13.用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮水处理的新技术。已知反应:
Fe2O3+3Na2O2
 2Na2FeO4+Na2O。下列说法正确的是( )
2Na2FeO4+Na2O。下列说法正确的是( )
A.Na2O2既是氧化剂又是还原剂
B.在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌
C.3mol Na2O2发生反应,有12mol电子转移
D.Na2FeO4既是氧化产物又是还原产物
12.下列实验方案可行的是( )
A.鉴别SO42-加入BaCl2溶液,再加稀盐酸,观察沉淀是否消失
B.证明CH2=CHCH2CHO中一定有碳碳不饱和键:滴入KMnO4酸性溶液,看紫红色
是否褪去
C.量取14.80mL 1mol·L-1NaOH溶液:选用25mL碱式滴定管
D.检验溶液中一定有CO32-:加入稀盐酸,将产生的气体通入澄清石灰水
11.下列说法不正确的是( )
A.100℃时,纯水中c(H+)=1×10-6mol·L-1,pH小于7,此时纯水显酸性
B.pH=12的烧碱和氢氧化钡溶液,二者物质的量浓度之比为2∶1
C.pH=3的盐酸与pH=5的硫酸等体积混合,pH=3.3
D.0.1mol·L-1CH3COOH溶液中;c(CH3COOH)>c(CH3COO-)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com