
题目列表(包括答案和解析)
1.下列有关化学用语正确的是:
A.氮气的电子式: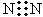 B.CS2的电子式:S=C=S
B.CS2的电子式:S=C=S
C.次氯酸钙的化学式:Ca(C1O)2
D.臭氧的化学式: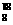 O
O
29.(13分)化学课外活动小组利用以下装置完成了系列实验,请回答以下问题
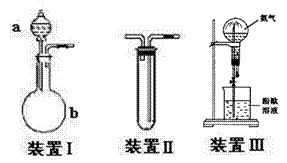 (1)甲同学用装置Ⅰ作为实验室制氧气的快速发生器,通过控制滴加a中溶液来控制产生气体的量,则a中放入的试剂为_______,b中放入的试剂为_______。(均填化学式)
(1)甲同学用装置Ⅰ作为实验室制氧气的快速发生器,通过控制滴加a中溶液来控制产生气体的量,则a中放入的试剂为_______,b中放入的试剂为_______。(均填化学式)
(2)乙同学把装置Ⅰ和装置Ⅱ联合,进行验证Cl2的氧化性比Br2强的实验,进行此项实验时在装置Ⅰ中的a中加入浓盐酸,b中加入高锰酸钾,装置Ⅱ中加入溴化钠溶液。则装置Ⅰ中反应的方程式为:___________________;根据装置Ⅱ中观察到的现象为________,说明Cl2的氧化性比Br2强。
(3)丙同学用装置Ⅰ制取NH3并由装置Ⅲ拟作喷泉实验。装置Ⅰ中a中加入浓氨水,b中加入CaO固体,可产生大量的氨气,回答下列问题:
①请用化学方程式表示浓氨水滴入CaO中有大量NH3逸出的过程:_____________________。
②检验NH3是否收集满的实验方法是:_____________________________________________。
(4)用装置Ⅲ进行喷泉实验,上部烧瓶已充满干燥氨气:
①引发水向上喷的操作是________________________________________________________,该实验说明了氨气的_______________________________________性质。
②若开始时测得装置Ⅲ烧瓶中NH3的质量是相同状况下相同体积H2质量的10倍,则喷泉实验完毕后,烧瓶中水可上升至烧瓶容积的__________(填“几分之几”)。
龙岩一中2009届高三第五次月考
28.(7分)某溶液由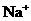 、
、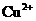 、
、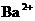 、
、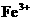 、
、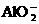 、H
、H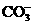 、
、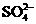 、
、 中的若干种离子组成.取适量该溶液进行如下实验:
中的若干种离子组成.取适量该溶液进行如下实验:
①向其中加入过量盐酸,有气体生成,并得到无色透明溶液;
②向①所得溶液中加入过量氨水,产生白色沉淀,过滤;
③向②所得滤液中加入过量氢氧化钡溶液,产生白色沉淀,过滤;
④向③所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀.
根据上述实验回答下列问题:
(1)原溶液中一定不存在的离子是_________________________________________;
(2)原溶液中一定存在的离子是___________________________________________。
27.(9分)X、Y、Z、W、N五种短周期主族元素的原子序数为X>W>Z>Y>N,W原子的最外层电子数是X原子最外层电子数的一半,Y是形成化合物种数最多的元素,Z原子次外层电子数是最外层电子数的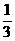 ,N元素原子半径是所有原子中最小的,这五种元素原子核电荷数总和为38。
,N元素原子半径是所有原子中最小的,这五种元素原子核电荷数总和为38。
(1)X________,Z_______(填元素符号)。
(2)这五种元素原子半径的大小为:__________>_______>_______>_______>_______(填元素符号)。
(3)W、X元素的最高价氧化物对应水化物的碱性强弱为______<______。(用化学式表示)
(4)写出由上述元素组成的具有漂白作用的三种物质的化学式_______、_______、_______。
(5)写出由Y、Z、W、N四种元素成的化合物溶于水,并与水反应的化学方程式_____________
__________________________________________________________________。
26.(6分)位于元素周期表第三、四两周期中的主族元素A和B,它们的离子相差两个电子层。已知A元素位于元素周期表中第m主族,B元素位于第n主族。那么:
(1)A元素原子的核外电子数为_______(用含m的代数式表示),其离子最外层电子数为_______;
(2)B元素原子的核内质子数为_______(用含n的代数式表示),其离子的电子数为_______;
(3)A、B两元素形成的化合物的化学式为AB2,其化学键类型为_______;
(4)用电子式表示AB2为_______。
25.在相同状况下将镁、铝、铁分别投入质量相等且足量的稀硫酸中,反应结束后,三种溶液的质量仍相等,则投入镁、铝、铁三种金属的质量关系正确的是 ( )
A.Mg > Al > Fe B.Al > Fe > Mg C.Al > Mg > Fe D.Fe > Mg > Al
24.臭氧可使湿润的KI淀粉试纸变蓝,反应式:2KI+O3+H2O==2KOH+I2+O2,下列说法正确的是 ( )
A.O3在反应中被氧化成O2 B.O2氧化能力大于O3
C.1molO3反应中得到2mol电子 D.氧化产物O2与还原产物I2的物质的量之比为1∶1
23.A、B、C、D是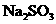 、
、 、HCl、
、HCl、 四种无色溶液中的某一种,把它们两两混合产生的现象是:A+B→白色沉淀;A+C→白色沉淀;B+C→白色沉淀;C+D→白色沉淀;B+D→无色、有刺激性气味的气体.则上述四种物质按A、B、C、D的顺序是( )
四种无色溶液中的某一种,把它们两两混合产生的现象是:A+B→白色沉淀;A+C→白色沉淀;B+C→白色沉淀;C+D→白色沉淀;B+D→无色、有刺激性气味的气体.则上述四种物质按A、B、C、D的顺序是( )
A. 、
、 、
、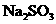 、HCl B.
、HCl B. 、HCl、
、HCl、 、
、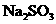
C.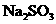 、HCl、
、HCl、 、
、 D.
D. 、
、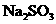 、
、 、HCl
、HCl
22.下列离子方程式正确的是 ( )
A.氯气通入水中:Cl2 + H2O == 2H++Cl-+ClO-
B.向偏铝酸钠溶液中通入过量的CO2气体:AlO2―+ 2H2O+CO2 == Al(OH)3+HCO3―
C.加热浓盐酸和二氧化锰的混合物:MnO2+4H++4Cl- Mn2++2H2O+2Cl2↑
Mn2++2H2O+2Cl2↑
D.向澄清的石灰水中加入少量NaHCO3:
Ca2++2OH―+2HCO3―==CaCO3↓+2H2O+CO32―
21.FeS2的结构类似于Na2O2,是一种过硫化物,与酸反应生成H2S2。H2S2类似于H2O2,易分解:H2S2=H2S+S↓实验室用稀盐酸制H2S时,某学生误将FeS2颗粒当作FeS作用,当FeS2反应完后,不可能生成的物质是 ( )
A.H2S B.S C.FeS D.FeCl2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com