
题目列表(包括答案和解析)
3. 20 g AO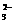 中核外电子数比质子数多0.5NA(NA代表阿伏加德罗常数)个,则元素A的相对原子质量为( B )
中核外电子数比质子数多0.5NA(NA代表阿伏加德罗常数)个,则元素A的相对原子质量为( B )
A. 12 B. 32 C. 60 D. 80
2. 下列溶剂能溶解单质碘和溴,但不能把碘和溴从碘水和溴水中萃取出来的是( D )
A. 汽油 B. 苯 C. 四氯化碳 D. 酒精
[解析] 萃取剂选择三原则①萃取剂和原溶液中的溶剂互不相溶②溶质在其中的溶解度较大③萃取后溶质和萃取剂容易分离。酒精易溶于水,不能分层。
1. 下列物质的保存方法,正确的是( C )
A. 保存液溴时,加少量水密封,敞口置于空气中
B. 氢氟酸保存在棕色玻璃试剂瓶中
C. 液氯密闭保存在干燥的钢瓶中
D. 新制氯水通常保存在无色试剂瓶中
22.( 1分) )氢气还原氧化铜的反应不完全时,便得到Cu、Cu2O、CuO的固体混合物。
化学兴趣小组同学为探究上述固体的成分进行了如下操作和实验:
(1)取一定质量的均匀固体混合物A,将其分成两等份。
(2)取其中-份用足量的氢气还原,测得反应后固体质量减少3.20g。
(3)另一份加入500mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气
体2.24L。
请回答以下问题:
(1)A中,n(Cu)+n(Cu2O)= 。
(2)A中,n(CuO)的取值范围是 。
(3)试计算所用稀硝酸的物质的量浓度(要求有计算过程)。
21.(12分)下面是甲、乙两同学对草酸受热分解及其产物的检验做的探究:
甲、乙两同学通过网络查询,获得草酸及草酸晶体的一些相关知识:
|
名称 |
分子式 |
颜色、状态 |
溶解性 |
|
熔点(℃) |
密度(g/cm3) |
|
草酸 |
H2C2O4 |
- |
易溶于水 |
|
189.5 |
1.900 |
|
草酸晶体 |
H2C2O4·2H2O |
无色晶体 |
- |
|
101.5 |
1.650 |
备注:草酸晶体失去结晶水后,175℃以上开始分解。
(1) 猜想与假设:
第一种:草酸分解产物是CO2和H2;
第二种:草酸分解产物是CO2、CO和H2O;
第三种:草酸分解产物是CO2和H2O。
(2) 实验装置的设计(图中铁架台略去)甲同学设计了如图1所示的装置。乙同学设计了如图2所示的装置。
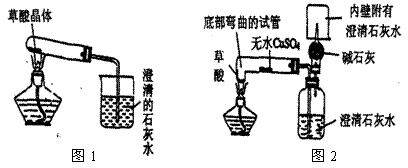
(3) 实验:
甲同学按图(1)装置实验,观察到澄清石灰水变浑浊,……
乙同学按图(2)装置实验,观察到:
A、无水CuSO4变蓝;
B、广口瓶中澄清石灰水变浑浊;
C、生成的气体通过碱石灰后,在尖嘴处点燃后能燃烧,在火焰上方罩一个内壁附有澄清石灰水的烧杯,澄清的石灰水变浑浊。证明产物中有 。
(4) 结论:
第 种猜想是正确的,请写出草酸受热分解的化学反应方程式
。
(5) 反思与评价
乙同学认为甲同学设计的实验装置有缺陷。由于试管口向下倾斜,而且草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中常会出现熔融的草酸流进导管而影响后续实验。甲同学认为乙同学的设计是科学合理的。请你谈谈图2装置优于图1装置之处:
第一点: 。
第二点: 。
第三点: 。
。
乙同学设计的图2装置也能证明产物中无H2,证明方法是
。
20.(8分)某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示,请回答:
|
检测次数 |
溶液中检测出的离子 |
|
第一次 |
KCl、K2SO4、Na2CO3、NaCl |
|
第二次 |
KCl、BaCl2、Na2SO4、K2CO3 |
|
第三次 |
Na2SO4、KCl、K2CO3、NaCl |
⑴三次检测结果中第 次检测结果不正确。
⑵在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子:
首先,向溶液中滴加 溶液(填化学式),其目的是
;其次,然后继续加入过量的该溶液,其目的
是 ;第三,过滤,向滤液中加入 溶液(填化学式),其目的是 ;
第四,过滤,再向滤液中加入__________溶液(填化学式),其目的是
。
19.(10分)已知D是单质,其他均是常见的化合物,它们之间的转化关系如下图所示,其中M(A)<M(B)。
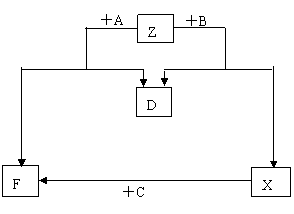
回答下列问题:
(1) 符合此转化关系的A、C的化学式分别是:A______________、C______________。
(2) 写出Z的电子式:_______________,Z中阴阳离子数之比为:_____________。
(3) 若向X的水溶液中滴加几滴酚酞试液,现象是 ,
出现此现象的原因用离子方程式表示为 ,然后再加入足量的BaCl2溶液,出现的现象是 ,原因是 。
(4) 室温下,将2g苯和过量的D混合,完全燃烧,放出83.6kJ的热量,写出苯燃烧热
的热化学方程式____________________________________________________。
18.(14分)正确书写电极反应和化学方程式:
(1)铁在潮湿的空气中转变为铁锈
负极: 正极:
总反应:
氧化反应:
分解反应:
(2)正确书写离子方程式
向FeBr2 溶液中加入少量Cl2
向FeBr2 溶液中加入足量Cl2
17.(6分)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、
H2O。已知水是反应产物之一。
(1)该反应中还原剂是 ;
(2)该反应中还原产物是 ;
(3)若反应过程中转移了0.3mol电子,则生成水的质量是 g。
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
|
|
|
|
|
|
|
|
|
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
|
|
|
|
|
|
|
|
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com