
题目列表(包括答案和解析)
35.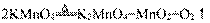 解决问题常面临着方法的选择,面对不同的结果我们应继续探索。为得知7克高锰酸钾完全分解能产生多少克氧气(化学反应方程式为:
),小柯与小妍分别采取了以下方法:
解决问题常面临着方法的选择,面对不同的结果我们应继续探索。为得知7克高锰酸钾完全分解能产生多少克氧气(化学反应方程式为:
),小柯与小妍分别采取了以下方法:
|
小柯:实验测定法 |
小妍:计算法 |
|
小柯在老师指导下,将7克高锰酸钾充分加热,得到氧气600厘米3。 |
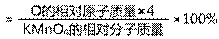 解:高锰酸钾中氧元素的质量分数 解:高锰酸钾中氧元素的质量分数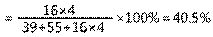 氧气的质量为7克×40.5%=2.84克 氧气的质量为7克×40.5%=2.84克答:7克高锰酸钾完全分解产生氧气2.84克 |
请回答:
(1)在本实验条件下氧气的密度为1.4×10-3克/厘米3,则由小柯的测量结果可以算出7克高锰酸钾分解后所产生的氧气质量为 ▲ 克。
(2)大家经过讨论,认为小妍的计算方法明显错误,此题不能采用该方法计算氧气质量的一项理由是 ▲ 。
A.高锰酸钾中含氧元素 B.锰酸钾和二氧化锰中含氧元素 C.氧气中含氧元素
(3)请通过化学方程式计算7克高锰酸钾完全分解所产生的氧气质量。
34.锌是人体生长发育、维持器官正常功能的微量元素,人体缺锌会引起多种疾病,因此缺锌者可通过服用葡萄糖酸锌等保健品来补锌。已知葡萄糖锌的化学式为C12H22O14Zn(相对分子质量为455)。请回答:
(1)葡萄糖酸锌是由___▲________种元素组成的。
(2)葡萄糖酸锌中所含锌元素的质量分数为多少?结果保留至0.1%)(2分)
(3)现有一支20mL的葡萄糖酸锌口服液,其中含锌6.5mg,那么该口服液中葡萄糖酸锌的质量是多少mg?(2分)
33.在一个密闭容器中放入A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下:
|
物质 |
A |
B |
C |
D |
|
反应前质量 (g) |
9 |
2 |
22 |
1 |
|
反应后质量(g) |
x |
2 |
6 |
21 |
⑴ 这一反应类型是 ▲ 反应; x= ▲ g。由表中数据分析可知,B可能没有参加该化学反应,也可能是该反应的 ▲ 剂。
⑵ 写出一例与上述反应类型相同的化学方程式: ▲ 。(2分)
32.目前,从能源消耗的构成看,我国及世界主要消耗的是煤.石油和天然气。
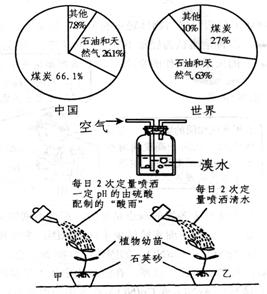 (1)右图是目前我国与世界能源的消费结构对比图。我国的这种能源消费结构对空气造成的污染十分严重。某校科学兴趣小组为测定校园附近空气中SO2的含量,采用如图所示的实验装置,反应的化学方程式为:
(1)右图是目前我国与世界能源的消费结构对比图。我国的这种能源消费结构对空气造成的污染十分严重。某校科学兴趣小组为测定校园附近空气中SO2的含量,采用如图所示的实验装置,反应的化学方程式为:
Br2+2H2O + SO2 = H2SO4 + 2HBr
(黄色) (无色)
实验中,当观察到_____▲ _____时,应立即停止通入空气。
(2)SO2是形成酸雨的主要原因之一。右图是小李设计的实验(除图中特别说明的外, 其他条件甲.乙均相同)。请据图推测:小李想探究的问题是 ▲ 。
(3) 我国的这种能源消费结构,燃烧过程产生的SO2遇到雨水成为酸雨。目前有一种较有效的方法,即用直升飞机喷洒碳酸钙粉末,脱硫效果可达85%。碳酸钙与SO2及空气中的氧气反应生成硫酸钙和二氧化碳,试写出该反应的化学方程式:_ _______▲____________。
31.小红为了探究“光合作用的条件和产物”,进行了如下图所示的实验操作(次序已打乱),请你结合所学知识回答下列有关问题:
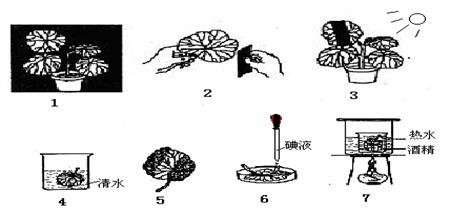
(1)该实验正确的操作步骤是1→3→2→ ▲ →5 。(用上图中的数字序号排列)
(2) 该实验探究的光合作用的条件是 ▲ 。
(3)小红的操作步骤完全正确,那么在上图5中可观察到的实验现象是 ▲ 。
30.某研究小组对用H2O2分解生成H2O和O2的实验条件进行探究。他们进行了以下实验,下列各图是气体的发生装置和收集装置示意图,请根据装置图回答下列问题:
(1)实验室用双氧水和二氧化锰来制氧气的发生装置应选用 ▲ (填装置的编号),如果要用E装置来收集氧气,则气体应从 ▲ (填字母)端通入。
(2)实验步骤:
① 往盛有5 mL 5 % H2O2溶液的试管中,伸入带火星的木条,木条不复燃。
② 往盛有5 mL w % H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃。
③ 往盛有5 mL w % H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃。
④ 经检验,②、③ 中反应后试管中仍分别含有a g MnO2和a g Fe2O3。
|
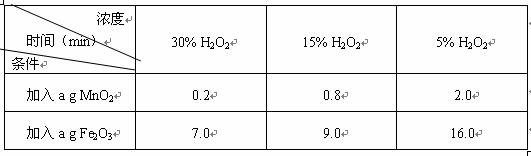
研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究。下表选取了部分实验数据:
用足量等体积H2O2溶液制取相同体积O2所需的时间
|
29.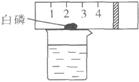 某同学设计了如右图的实验装置来测定空气中氧气的含量,图中烧杯中盛有80℃的热水,烧杯上方是一左端封闭按体积均匀划分刻度的玻璃管(已固定好),玻璃管内有一可左右滑动的活塞,活塞左侧玻璃管内封闭有空气,活塞右侧的玻璃管口跟空气相通,实验开始前活塞处于刻度5处。
某同学设计了如右图的实验装置来测定空气中氧气的含量,图中烧杯中盛有80℃的热水,烧杯上方是一左端封闭按体积均匀划分刻度的玻璃管(已固定好),玻璃管内有一可左右滑动的活塞,活塞左侧玻璃管内封闭有空气,活塞右侧的玻璃管口跟空气相通,实验开始前活塞处于刻度5处。
(1)实验结束后,玻璃管内发生的现象是:
活塞向____▲____移动。(填“左”“右”或“不”)
(2)恢复至室温后,活塞应停留在刻度_____▲_____处。
28.环境问题是人类可持续发展必须解决的一个重要问题,温室效应被列为21世纪人类面临的最大威胁之一,已引起人们的广泛关注。旨在限制发达国家温室气体排放量、抑制全球范围内气候持续变暖的《京都议定书》,已于2005年2月16日正式生效。
(1)二氧化碳是大气中的主要温室气体,我国二氧化碳的排放量位居世界第二,为减少二氧化碳这种温室气体的排放,我们可以采取的措施有(只要合理就得分):
▲ 。
(2)为减缓二氧化碳使全球变暖的趋势,有科学家提出大胆设想:将排放到空气中的二氧化碳压缩使其液化,然后将其压入到冰冷的深海中。但也有科学家担心海水中富含二氧化碳后酸度会增加,可能会杀死一些海洋生物,甚至会溶解掉部分海床,同时气候变化也可能改变海洋环流,把海底的二氧化碳又带回海面,另外把二氧化碳压入海底所消耗的能源可能会再增加二氧化碳的排放。
①二氧化碳气体转变为液体时将会 ▲ 能量(填“释放”或“消耗”);
②二氧化碳使海水酸度增加的原理用化学方程式表示为: ▲ ;
③二氧化碳在深海中的溶解度比在通常状况下的水中的溶解度 ▲ ,原因是 ▲
27.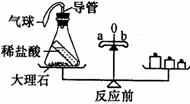 小明设计了一个实验来探究质量守恒定律。如图所示,反应前天平平衡,他取下此装置
(装置气密性良好)将其倾斜,使稀盐酸(HCl)和大理石(主要成分是碳酸钙)接触,生成氯化钙.二氧化碳气体和水,待充分反应后,气球膨胀,再将装置放回天平左盘,此时他发现天平的指针向右偏转了。请问:
小明设计了一个实验来探究质量守恒定律。如图所示,反应前天平平衡,他取下此装置
(装置气密性良好)将其倾斜,使稀盐酸(HCl)和大理石(主要成分是碳酸钙)接触,生成氯化钙.二氧化碳气体和水,待充分反应后,气球膨胀,再将装置放回天平左盘,此时他发现天平的指针向右偏转了。请问:
(1)这一现象是否遵守质量守恒定律? ▲ ;
(2)为什么天平失去平衡? ▲ 。
(3)用上述原理来探究质量守恒定律,应在 ▲ 条件下实验。
26.目前有些人热衷于利用高压氧舱、氧吧、氧气袋等进行吸氧,以增加大脑供氧量,消除脑疲劳。医生建议吸氧要适量,因为高浓度的氧往往会对人造成伤害,引起氧中毒。
(1)氧气的化学性质活泼,具有______▲______性,能将人体内的有机物氧化分解成二氧化碳和水,同时释放出____▲________供生命活动所需。
(2)小红利用收集到的一瓶氧气,按下图中A、B、C、D的实验步骤进行实验,请写出实验步骤D中出现的现象 ▲ 。


A夹取炭 B点燃炭 C炭在氧气中燃烧 D.注入澄清石灰水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com