
题目列表(包括答案和解析)
7. (1) C; O; Na; S; Cl
(2) 略
(3)2Na2O2 + 2CO2 = 2Na2CO3 + O2





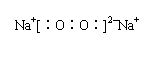
6. (1) O, Na, Al, Cl (2) AlCl3, Na2O2
(3)4AlCl3 + 6Na2O2 + 6H2O = 4Al(OH)3↓+ 12NaCl + 3O2 ↑
(4)Al3+ + 3AlO2– + 6H2O = 4Al(OH)3 ↓
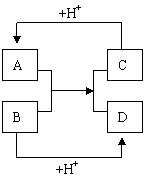
5.A、B、C、D分别是由两种短周期元素组成
的常见微粒(或粒子),这四种微粒中均含有相
同数目的电子,且共含有三种元素。其中A中
含有5个原子核,它们之间有如图的反应关系:
(1)A、D的电子式分别为: A ,
B 。
(2)B、C、D三种微粒结合质子能力x > y > z,(x、y、z
分别代表B、C、D中的某一种微粒), 则x、y、z分别
代表的微粒符号为x , y , z 。
专题(四)答案例题:1B 例题2 :(1)N2, CO; CO2, N2O (2)O3, SO2
课堂练习:
|
1A |
2C |
3A |
4A |
5B |
4.有位于20号元素前, 原子叙述依次递增的A、B、C、D、E五种元素。A、C元素的电子层数相同;A、E两元素的最外层和次外层电子数相同; A和C可形成化合物AC,D和E可形成ED2;B元素的原子最外层即M层有3个电子。
(1)试写出这五种元素的名称及符号:A 、 B 、
C 、D 、E 。
(2)写出下列反应的化学反应式:
①A+C→AC
②D+E→ED2
3.某主族元素的离子X2+有6个电子层,最外层有2个电子,当把XO2溶于浓盐酸时,有黄绿色气体产生,则下列说法正确的是 ( )
A.X2+具有强还原性 B.XCl2溶液呈中性
C.XO2具有强氧化性 D.该元素是ⅡA族
2.元素周期表对工农业生产具有一定的指导作用,下列说法中不正确的是 ( )
A. 通常农药中所含的元素位于周期表右上角
B. 半导体材料在金属元素和非金属元素分界线附近
C. 在过渡元素中可以寻找新型催化剂材料
D.在IA族元素中寻找新型耐高温耐腐蚀的材料
1.下列叙述正确的是 ( )
A.同周期元素中,ⅦA族元素的原子半径最大
B.现已发现的零族元素的单质在常温常压下均为气体
C.ⅥA族元素的原子,其半径越大,越容易得到电子
D.所有的主族元素的简单离子的化合价与其族序数相等
8.已知A、B、C、D均为短周期元素,它们的原子序数依次递增。 A是最外层为一个电子的非金属元素,C 原子的最外层电子数是次外层的3倍; C和D可形成两种固态化合物,其中一种为淡黄色固体;B和C可形成多种气态化合物。A、B、C三种元素可以形成离子晶体,该晶体中各元素原子的物质的量之比为A:B:C=4:2:3。请回答下列问题:
(1)写出B的原子结构示意图 ,写出C和D形成的淡黄色固体化合物的电子式 。
(2)元素原子的物质的量之比为A:B:C=4:2:3 的晶体名称为 , 其水溶液显 性,其反应的离子方程式为 。
(3)请写出A2C和BA3分子中电子数相同,且仍由A、B、C元素中任意两种元素组成的微粒的符号(举两例) 、 。
(4)写出由B、C元素组成且元素原子质量比为B:C=7:12的化合物的化学式 。
课后练习:
7.A、B、C、D、E五种元素,已知:
(a)A 原子最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E 原子M层上的电子比K层多5个。
(b)常温下B2是气体,它对氢气的密度为16。
(c)C单质在B2燃烧,生成淡黄色固体。F与AB2反应可生成B2。
(d)D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2。
(1)A是 ,B是 ,C是 , D是 ,
E是 。(写元素符号)
(2)E的原子结构示意图: ;C的离子结构示意图: 。
(3)F与AB2反应的方程式: 。
6. A、B、C、D是20号以内的四种元素,其原子序数依次增大。C和D可形成化合物X,A和B可形成化合物Y,将少量X和过量Y一起放入水中,可放出一种无色无味的气体,同时得到一种无色澄清的溶液。向此溶液中滴加过量X的水溶液时,可生成一种白色胶状沉淀物Z(Z与Y的相对原子质量相等)。过滤后得到一种无色澄清溶液,其中含G,G的焰色呈黄色,向G的水溶液中加入酸化的硝酸银溶液时,能生成一种白色沉淀。根据以上推断:
(1)A是 ,B是 ,C是 ,D是 。
(2)X的分子式是 ,Y的化学式是 。
(3)4 mol X与6 mol Y在水溶液中发生反应的化学方程式是 。
(4)生成白色胶状沉淀物Z的离子方程式是: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com