
题目列表(包括答案和解析)
11.取相同体积的KI、Na2S、FeBr2溶液,分别通入足量的Cl2,当反应恰好完成时,消耗Cl2的体积相同(同温、同压条件下),则KI、Na2S、FeBr2溶液的物质的量浓度之比是
A.1:1:2 B.2:1:3 C.6:3:2 D.3:2:1
10.氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性,下列叙述中不正确的是
A.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟
B.钠在氯气中燃烧,生成白色的烟
C.纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现白色烟雾。
D.氯气能与水反应生成次氯酸和盐酸,久置氯水最终变为稀盐酸
9.R、Q为短周期中的两种元素,R元素原子的最外层电子数与次外层电子数之差的绝 对值等于电子层数;Q元素的原子比R元素的原子多2个核外电子,则下列叙述中肯定不正确的是
A.原子半径:R>Q B.R和Q可形成离子化合物
C.R和Q可形成共价化合物RQ2 D.R和Q可形成共价化合物RQ3
8.在相同条件下,A容器中的O2和B容器中的NH3所含的原子总数相等,则两个容器的
体积比为
A.1:2 B.1:3 C.2:3 D.2:1
7.下列叙述中,正确的是
A.含金属元素的离子一定都是阳离子
B.在氧化还原反应中,非金属单质一定是氧化剂
C.金属阳离子被还原不一定得到金属单质
D.某元素从化合态变为游离态时,该元素一定被还原
6.下列有关Na2CO3和NaHCO3性质的比较中,不正确的是
A.对热稳定性:Na2CO3 >NaHCO3 B.常温时水溶性:Na2CO3 >NaHCO3
C.与稀盐酸反应的快慢:Na2CO3 >NaHCO3 D.相对分子质量:Na2CO3>NaHCO3
5.在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:
3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M
关于该反应的说法中正确的组合是
① 氧化剂是H3AsO3 ② 还原性:Cl->As;③ 每生成1molAs,反应中转移电子的物质的量为3mol;④ M为OH-;⑤ SnCl62-是氧化产物。
A.①③⑤ B.①②④⑤ C.①②③④ D.只有①③
4.下列有关离子大量共存的说法正确的是
A. S2-、Na+、Fe3+、SO42-能大量共存
B.水电离产生c(H+)=1×10-12mol/L的溶液中,可能有Mg2+、Na+、Cl-、HCO3大量共存
C.澄清透明的溶液中,可能有Ba2+、Cl-、Al3+、SO42-大量共存
D.在K+、AlO2-、Cl-、SO42- 溶液中加入过量Na2O2后仍能大量共存
3.下列关于热化学反应的描述中正确的是
A.需要加热才能发生的反应一定是吸热反应
B.当反应物的总能量比生成物的总能量高时,为放热反应;当生成物的总能量比反应物的能量高时,则表现为吸热反应。
C.CO(g)的燃烧热是283.0 kJ·mol-1,则CO(g)的燃烧热的热化学方程式为:
2CO(g)+O2(g) =2CO2(g);ΔH=-566 kJ·mol-1
D.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则1molH2SO4和1molBa(OH)2反应放出的热量为114.6kJ
2. 化学科学需要借助化学专用语言描述,下列有关化学用语正确的是
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是
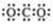 A.CO2的电子式 B. Cl-的结构示意图
A.CO2的电子式 B. Cl-的结构示意图
C.氢有三种同位素: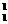 H、
H、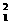 H、
H、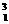 H,故可形成三种分子
H,故可形成三种分子
D.氧气和臭氧、红磷和白磷、普通水和重水互称为同素异形体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com