
题目列表(包括答案和解析)
37.(6分)A、B、C、D、E为原子序数依次增大的主族元素,已知A、B、E三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3,回答:
(1)写出下列元素符号:A______________,E______________,D______________。
(2)写出A、B两元素最高价氧化物的水化物相互反应的化学方程式_____________A、E两元素最高价氧化物的水化物相互反应的化学方程式______________________。
(3)比较D、E最高价氧化物对应水化物的酸性。
36.(6分)现有A、B、C三种元素,已知它们的最外层电子数之和等于氧原子最外层电子数,其核内质子数之和不超过18,将它们分别跟O元素结合,均可生成两种氧化物;A+O2→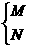 ,B+O2→
,B+O2→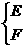 ,C+O2→
,C+O2→ ,两种氧化物中氧元素质量分数:N>M,E>F,Y>X。M跟X化合,其生成物D可与E形成两种化合物P和Q,其中Q可用来治疗胃酸过多的疾病。据此推断下列元素或化合物(用元素符号或化学式表达)
,两种氧化物中氧元素质量分数:N>M,E>F,Y>X。M跟X化合,其生成物D可与E形成两种化合物P和Q,其中Q可用来治疗胃酸过多的疾病。据此推断下列元素或化合物(用元素符号或化学式表达)
A______________,B______________,C______________;M______________,N______________,E______________,F______________,X______________,Y______________;P______________,Q______________。
35.(6分)W、X、Y、Z四种元素的核电荷数均小于18,且依次递增,W原子核内仅有一个质子,X原子的电子总数与Z原子最外层电子数相等,W原子与X原子的最外层电子数之和与Y原子的最外层电子数相等,Z原子L层电子数是K层电子数的3倍,且Z能形成阴离子,由此推断它们的元素符号:W______________,X______________,Y______________,Z______________已知W、X、Z和W、Y、Z分别可组成化合物,其化学式分别为______________、______________。
34.(3分)有两种气体单质Am和Bn,已知2.4gAm和2.1gBn所含原子个数相同,分子个数比却为2∶3,又知A和B原子核内质子数都等于中子数,且A原子中L电子层所含电子数是K电子层的3倍,试推断:
(1)元素符号:A______________,B______________;
(2)Am中m值是______________。
33.(6分)A、B、C、D四种元素都是短周期元素。A元素的离子具有黄色的焰色反应。B元素的离子结构和Ne具有相同的电子层排布;5.8gB的氢氧化物恰好能与100mL2mol/L盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构里,最外层电子数是次外层电子数的3倍。根据上述条件,回答:
(1)元素C位于第______________周期______________族,它的最高价氧化物的化学式为______________。
(2)A是______________元素,B是______________元素,D是______________元素。
(3)A与D形成稳定的化合物的化学式为______________,判断该化合物在空气中是否变质的简单方法是______________。
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为______________。
32.(6分)不同元素的气态原子失去最外层的1个电子所需要的能量(设其为E)如下图所示。试根据元素在周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
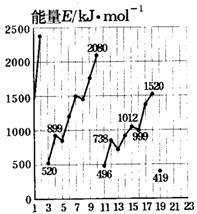
原子序数1至19号元素气态原子失去最外层的1个电子所需能量
(1)同主族内不同元素的E值变化的特点是:______________。各主族中E值的这种变化特点体现了元素性质的______________变化规律。
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象。试预测下列关系式中正确的是______________。(填写编号,多选倒扣分)
①E(砷)>E(硒)
②E(砷)<E(硒)
③E(溴)>E(硒)
④E(溴)<E(硒)
(3)估计1mol气态Ca原子失去最外层的1个电子所需能量E值的范围:______________<E<______________。
(4)10号元素E值较大的原因是__________________________________。
31.(5分)A、B两种离子具有相同的电子层,A、B两元素的单质都能与水剧烈反应,在反应中A单质为氧化剂,B单质为还原剂。则:
(1)A离子的结构示意图为______________,B原子的结构示意图为______________。
(2)A元素位于______________周期______________族。新发现A的一种含氧酸的化学式为HAO,其中A的化合价为______________。
(3)A单质与水反应的化学方程式为______________。
(4)B单质与水反应的离子方程式为______________。
30.属于短周期的A、B元素,A的原子半径小于B的原子半径,两元素可形成A显正价的AB2型化合物,下列有关A、B两元素的叙述中正确的是( )
A.A、B可能属于同一周期
B.A是B的前一周期元素
C.A只可能是金属元素
D.A可能是第二周期中ⅣA族或ⅡA族元素
29.在两种短周期元素组成的化合物中,若它们的原子个数之比为1∶3,设两种元素的原子序数分别为a和b,则下列对a和b可能的关系概括得最完全的是( )
①a=b+5 ②a+b=8 ③a+b=30 ④a=b+8
A.只有②③ B.只有②③④
C.只有③④ D.①②③④
28.A、B是同主族的相邻元素,A所在周期共有m种元素,B所在的周期共有n种元素,且m>n,若A的原子序数为x,则B的原子序数可能是( )
①x+m ②x-m ③x+n ④x-n
A.①③ B.②④ C.②③ D.①④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com