
题目列表(包括答案和解析)
9.用下列装置能达到有关实验目的的是

甲 乙 丙 丁
A.用甲图装置电解精炼铝 B.用乙图装置制备Fe(OH)2
C.丙图装置可制得金属锰 D.丁图验证NaHCO3和Na2CO3热稳定性
8.下列各组离子在指定条件下,-定能大量共存的是
A.在c(H+)/c(OH-)=1×1012的溶液中:I-、Cl-、HCO3-、Na+
B.pH=1的溶液中:Cu2+、Al3+、SO42-、NO3-
C.能使碘化钾淀粉试纸变蓝的溶液中:Na+、NH4+、S2-、Br-
D.水电离出的c(H+)=10-12mol/L的溶液中:Na+、Mg2+、Cl-、S2-
不定项选择题(本题包括6小题,每小题4分,共24分。每小题有一个或二个选项符合
题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,
只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就为0分)
7.A、B、C和D都是周期表中前20号元素,已知A的阳离子和C的阴离子具有相同的核外电子排布,且能形成组成为AC的化合物;C和D属同族元素,其中C中核外电子数是D中核内质子数的2倍。B和D是同周期元素且A和B能形成AB2型化合物。下列说法中正确的是
A.D元素处于元素周期表中第2周期第Ⅵ族 B.AB2中可能既有离子键又有共价键
C.四种元素的原子半径A>C>D>B D.BC2分子一定是极性分子
6.盖斯定律认为:不管化学过程是一步或分为数步完成,这个过程的热效应是相同的。
已知:H2O(g)= H2O(l) △H1 =-Q1kJ·mol-1(Q1>0)
C2H5OH(g)= C2H5OH(l) △H2 =-Q2kJ·mol-1(Q2>0)
C2H5OH(g)+3O2(g)= 2CO2(g)+3H2O(g) △H3 = -Q3kJ·mol-1(Q3>0)
若使23g液态乙醇完全燃烧,最后恢复到室温,则放出的热量为(kJ)七彩教育网 A.Q1+ Q2+Q3 B.0.5(Q1+Q2+Q3 )
C.0.5 Q1-1.5 Q2+0.5Q3 D.1.5 Q1-0.5 Q2+0.5Q3
5.LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠。已知该电池放电时的电极反应式为:正极 FePO4+Li++e-==LiFePO4 负极 Li-e-== Li+
下列说法中正确的是
A.充电时电池反应为FePO4+Li = LiFePO4
B.充电时动力电池上标注“+”的电极应与外接电源的正极相连
C.放电时电池内部Li+向负极移动
D.放电时,在正极上是Li+得电子被还原
4.下列对实验现象的预测不正确的是
A.向Na2SiO3溶液中通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失
B.向氢氧化铁胶体中滴加盐酸至过量,开始有沉淀出现,后来沉淀又溶解
C.向Ca(ClO)2溶液中通入CO2,溶液变浑浊,再加入品红溶液,红色褪去
D.向Ca(OH)2溶液中通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入过量NaOH溶液,又变浑浊
3.NA代表阿伏加德罗常数。下列说法中,不正确的是
A.2.8g 乙烯与丙烯的混合物中含碳原子的数目为 0.2NA
B.25℃时,l L pH=13的Ba(OH)2 溶液中含有OH―的数目为0.1 NA
C.1 mol C30H62 分子中含有共价键的数目为 91 NA
D.标准状况下,NO和 O2各11.2 L 混合,所得混合气体的分子总数为 0.75 NA
2.化学是以实验为基础的学科,化学实验设计和操作中必须十分重视师生的安全问题和环境保护问题。下列操作方法不正确的是
A.制氧气时排水法收集氧气后出现倒吸现象,立即松开试管上的橡皮塞
B.实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
C.在气体发生装置上直接点燃乙炔气体时,必须先检验乙炔气体的纯度
D.给试管中的液体加热时不停移动试管或加入碎瓷片,以免暴沸伤人
1.下列有关化工生产的叙述中正确的是七彩教育网
A.将煤液化、气化,有利于提高燃料的燃烧效率
B.侯氏制碱法,向饱和NaCl溶液中先通入CO2再通入氨气制取纯碱
C.电解精炼铜时,同一时间内阳极溶解铜的质量与阴极析出铜的质量相等
D.工业生产硫酸中,建立高烟囱可以降低地面SO2的浓度,减少空气污染
(二)滤液含量的测定:
以下是该小组探究滤液的一个实验流程:
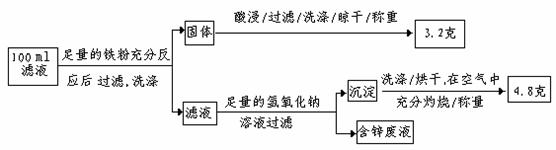
则100mL滤液中:①Cu2+ 的浓度为 mol·L-1 ;②Fe2+的浓度为 mol·L-1。
24.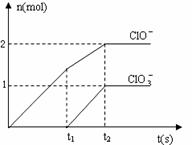 (8分)在一定量的石灰乳中通入一定量
(8分)在一定量的石灰乳中通入一定量
的氯气,二者恰好完全反应(发生的反应
均为放热反应)。生成物中含有Cl-、C1O-、
C1O3-三种含氯元素的离子,其中C1O-、
C1O3-两种离子的物质的量(n)与反应时
间(t)的曲线如右图所示。
(1)t2时,Ca(OH)2与Cl2发生反应的总的化
学方程式为:________________ 。
(2)该石灰乳中含有Ca(OH)2的物质的量是______ mol。
(3)据分析,生成Ca(C1O3)2的反应是由温度升高引起的,通入Cl2的速度不同,C1O-和C1O3-的比例也不同。在原石灰乳中:
Ⅰ 若通入氯气的速度加快,则反应后 _____2(填“>”、“<”或“=”);
_____2(填“>”、“<”或“=”);
Ⅱ 若 ,则n(C1-)=
mol(用含a的代数式来表示)。
,则n(C1-)=
mol(用含a的代数式来表示)。
锦州市2009届普通高中高三上学期期末考试
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com