
题目列表(包括答案和解析)
5.下列实验操作正确的是 ( )
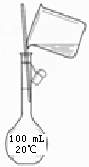
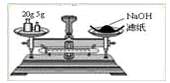
A.称量氢氧化钠固体 B.配制150mL0.10mol/L盐酸
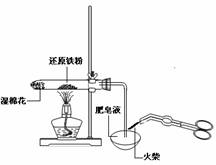
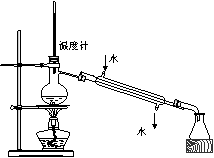
C.检验铁粉与水蒸气反应产生的氢气 D.分离两种互溶但沸点相差较大的液体混合物
4.下列说法正确的是( )
A.二氧化碳分子中存在共价键和分子间作用力
B.甲烷、氨和水都是由极性键结合而成的极性分子
C.同主族不同元素的最高价氧化物,一定具有相同的晶体结构
D.氟化氢的沸点高于氯化氢的沸点,正丁烷的沸点高于异丁烷的沸点
3.某物质溶于水,所得溶液既能使蓝色石蕊试纸变红,也能与碳酸盐反应生成气体,此物质有可能是:①氧化物 ②盐 ③碱 ④单质 ⑤酸 ( )
A.①②④ B.①②④⑤ C.② D.①②③④⑤
2.随着科学技术的不断进步,研究物质的手段和途径越来越多,N5+、H3、O4、C60等已被发现。下列有关说法中,正确的是 ( )
A.N5+离子中含有36个电子 B.O2与O4属于同位素
C.C60是原子晶体 D.H2与H3属于同素异形体
1.下列各组物质中都属于纯净物的是( )
A.福尔马林、水、醋酸 B.盐酸、二氧化碳、胆矾
C.明矾、四氧化三铁、碱式碳酸铜 D.苯、汽油、酒精
20.(9分)在Cu +
2H2SO4(浓)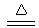 CuSO4 + SO2↑+ 2H2O反应中,
CuSO4 + SO2↑+ 2H2O反应中,
(1) 元素被氧化, 是氧化剂。
(2)用双线桥标出该反应电子转移的方向和数目。
Cu + 2H2SO4(浓) CuSO4 + SO2↑+ 2H2O
CuSO4 + SO2↑+ 2H2O
(3)某一反应体系有反应物和生成物的粒子共六种:SO32-、I2、H+、SO42-、I-、H2O。已知该反应中I2只发生如下过程:I2 →I-,请回答:
(1)该反应中的还原剂是 (填分子或离子符号)
(2)写出该反应的离子方程式
19.(18分)在一定条件下可实现下图所示物质之间的变化。其中甲、乙是生活中最常见的金属,丙是气体单质,其它字母表示化合物,其中A是红棕色固体。
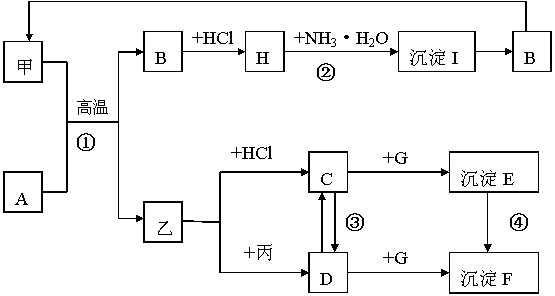
请填
填写下列空白: (1)单质乙的化学式是 ,其在周期表中的位置是 ; (2)写出反应②、③的离子方程式
②
③ (3)反应①的化学方程式是
(4)反应④过程中看到的现象是 。
(5)检验D中阳离子的方法是
。
18.(15分)A、B、C、D、 E五种短周期元素,它们的原子序数依次增大。A元素原子的电子层数等于核外电子总数,B原子的最外层电子数是电子层数的2倍,C的最高价氧化物对应的水化物与其氢化物反应生成一种盐X,元素D是地壳中含量最多的元素,A与E同主族。
(1)写出元素的名称:C_______________,E_______________
(2)画出D的原子结构示意图___________________________
(3)B的最高价氧化物的电子式是____________________________
(4)盐X的水溶液显酸性原因是_________________________________ (用离子方程式说明)。
17.(10分)
(1)可逆反应2SO2(g) + O2(g)  2SO3(g);△H<0,在其他条件不变时,
2SO3(g);△H<0,在其他条件不变时,
①升温反应速率___________, 增大压强反应速率___________;
②达到化学平衡时, V正(SO2) ________V逆(SO3)(填大于、小于、等于);若平衡后增加O2的浓度平衡向____ __ __方向移动,SO2的转化率 ;若升高温度,则平衡向___ ___ __方向移动。
(2) 将等物质的量的A、B、C、D四种物质混和,发生如下反应:
aA+bB  cC(固)+dD,
cC(固)+dD,
当反应进行一定时间后,测得A减少了n摩,B减少了1/2n摩,C增加了3/2n摩,D增加了n摩,此时达到化学平衡, 该化学方程式中各物质的系数为:
a =________、 b=________、 c=________、 d=________。
21.(14分)纯净的过氧化钙(CaO2)是白色的粉末,难溶于水,不溶于乙醇、乙醚,常温
下较为稳定,是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。
在实验室可用钙盐制取CaO2·8H2O,再经脱水制得CaO2。CaO2·8H2O在0℃时稳定,
在室温时经过几天就分解,加热至130℃时逐渐变为无水CaO2。
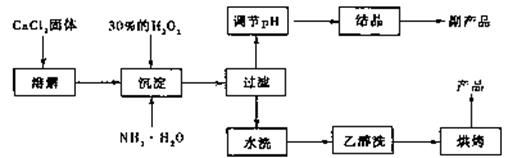 其制备过程如下:
其制备过程如下:
(1)用化学方程式表示出过氧化钙用做水产养殖增氧剂的原理:
。
(2)为了控制沉淀温度为0℃左右,在实验室宜采取的方法是 。
(3)该制法的副产品为 (填化学式),为了提高副产品的产率,结晶前要将
溶液的pH调整到合适范围,可加入下列试剂中的 (填写A或B)。
A.盐酸 B.氨水
(4)为了检验“水洗”是否合格,可取少量洗涤液于试管中,再滴加
进行检查。
(5)测定产品中CaO2的含量的实验步骤是:
第一步,准确称取ag产品于有塞锥形瓶中,加入适量蒸馏水和过量的bgKI晶体,再滴
入少量2 mol·L-1的H2SO4溶液,充分反应。
第二步,向上述锥形瓶中加入几滴淀粉溶液。
第三步,逐滴加入浓度为c mol·L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液VmL。
(已知:I2+2S2O32-===2I-+S4O62-(无色))
①第三步中说明反应恰好完全的现象是 ;
②CaO2的质量分数为 (用字母表示)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com