
题目列表(包括答案和解析)
16.下列实验操作处理,能有效改变反应速率且达到变化要求的是 ( )
A.为增大泡沫灭火器中Al2(SO4)3 与小苏打的反应速率,改用小苏打和苏打的混合物
B.加快盐酸和锌制取氢气的速率又不减少氢气的量,可加少量硝酸铜溶液
C.在稀硫酸和铁粉反应制取氢气时,为减慢反应速率,可加入适量醋酸钠
D.用3mL乙醇、2mL浓H2SO4、2mL冰醋酸制乙酸乙酯,为增大反应速率,现改用6mL乙醇、4mL浓H2SO4、4mL冰醋酸
15.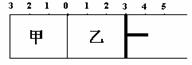 如图所示,甲容器容积固定不变,乙容器有可移动的
如图所示,甲容器容积固定不变,乙容器有可移动的
活塞。甲中充入2 mol SO2和1mol O2,乙中充入
2 mol SO3和1mol He,在恒定温度和催化剂条件下,
甲、乙达到如下平衡:
2SO3(g) 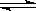 2SO2(g)+ O2 (g)。根据活塞位置,
2SO2(g)+ O2 (g)。根据活塞位置,
下列有关说法正确的是 ( )
A.若活塞固定在3处不动,达平衡时两容器中的压强相等
B.若活塞固定在3处不动,达平衡时两容器中SO3的浓度相等
C.若活塞固定在4处不动,达平衡时两容器中SO3的物质的量分数相等
D.若活塞固定在5处不动,达平衡时乙容器中SO2的物质的量较小
14.现有含21.2gNa2CO3的溶液和60g溶质质量分数为18.25%的盐酸,欲用这两种药品制取CO2。甲方案:向Na2CO3溶液中逐滴加入盐酸。乙方案:向盐酸中逐滴加入Na2CO3溶液。用两种方案制得的CO2可能是 ( )
A.2.2g B.4.4g C.6.6g D.8.8g
13.阿伏加德罗常数为6.02×1023mol-1,下列说法中正确的是 ( )
A.1molNO2气体与水反应生成的NO3-离子数目为6.02×1023
B.7.8g Na2O2中含有的离子总数为0.3×6.02×1023
C.0.1molCnH2n+2中含有的C-C键数为0.1n×6.02×1023
D.标准状况下,2.24LCHCl3含有的分子数为0.1×6.02×1023
12.现有乳酸(CH3―CH―COOH)和乙醇的混合物共1mol,完全燃烧生成54g水和56LCO2(标准状况下测定),则其消耗氧气的物质的量为 ( )
A.2 mol B.2.25 mol C.3 mol D.3.75 mol
11.向1mol炽热的Cu2S通入足量的水蒸气,充分反应后生成2mol H2,则Cu2S应转化为
( )
A.Cu和SO2 B.Cu和S C.CuO和SO2 D.Cu2O和S
10.世界卫生组织推荐的人类食用油脂肪酸标准为:饱和脂肪酸:单不饱和脂肪酸:多不饱和脂肪酸=1:1:1(物质的量之比),下列选项中按饱和脂肪酸、单不饱和脂肪酸、多不饱和脂肪酸顺序排列的是:①C17H35COOH ②C17H33COOH ③C15H31COOH ④C17H31COOH ⑤C17H29COOH ( )
A.②④⑤ B.③②④ C.②③④ D.①⑤③
9.下列各组物质在适宜的条件下反应,其中氧化剂与还原剂物质的量之比为2﹕1的是
A.H2SO4(浓)+C B.Fe2O3+Al
C.Cl2+Mg D.NO2+H2O
8.将两种硫酸盐按一定比例混合后共熔,可制得化合物X,X溶于水能电离出K+、Cr3+、SO42-,若将2.83 g X中的Cr3+全部氧化为Cr2O72-后,溶液中的Cr2O72-可和过量KI溶液反应,得到3.81 g I2,反应的离子方程式为:Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,若向溶有2.83 g X的溶液中,加入过量的BaCl2溶液,可得到4.66 g白色沉淀。由此可推断出X的化学式为 ( )
A.K2SO4·2Cr2(SO4)3 B.2K2SO4·Cr2(SO4)3
C.K2SO4·Cr2(SO4)3 D.K2SO4·1/2Cr2(SO4)3
7.短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍,是Y原子最外层电子数的3倍。下列说法正确的是 ( )
A.X的氢化物溶于水显酸性
B.Y的氧化物是离子化合物
C.Z的氢化物比H2O稳定
D.X和Z的氧化物对应的水化物都是强酸
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com