
题目列表(包括答案和解析)
4、某溶液中存在Na+、SO42-、SO32-、Cl-、HCO3-、Br-中的若干种,依次进行下列实验:
(1)用pH试纸检验,溶液的pH>7;
(2)向溶液中滴加新制氯水,无气体产生,加入四氯化碳振荡、静置,四氯化碳层呈橙色,
用分液漏斗分液;
(3)向分液后所得的水溶液中加入硝酸钡和稀硝酸的混合液,只有白色沉淀产生,过滤;
(4)在滤液中加入硝酸银和稀硝酸的混合液,有白色沉淀产生。
下列判断正确的是( ) ①肯定有Na+ ②肯定有SO42- ③肯定有SO32-
④肯定有Br- ⑤肯定有Cl- ⑥肯定没有HCO3-
A.①③④⑥ B.①②④⑥ C.②③④⑥ D.③④⑤⑥
3、用惰性电极电解一定量的CuSO4溶液,下列说法中,正确的是
A.阳极发生的电极反应为:Cu2+ + 2e- =Cu
B.阴极发生的电极反应为;4OH- =2H2O + O2↑+ 4e―
C.若有6.4g金属Cu析出,放出的O2一定为0.05 mol
D.电解完成后,加入一定量的Cu(OH)2,溶液可能恢复到原来的浓度
2.世界著名的科技史专家、英国剑桥大学的李约瑟博士考证说:“中国至少在距今3000年以前,就已经使用玻璃了。”下列有关玻璃的说法不正确的是
A.制普通玻璃的原料主要是纯碱、石灰石和石英 B.玻璃很硬属于原子晶体
C.普通玻璃的成分主要是硅酸钠、硅酸钙和二氧化硅
D.盛放烧碱溶液的试剂瓶不能用玻璃塞,是为了防止烧碱跟二氧化硅生成硅酸钠而使瓶塞与瓶口粘在一起
1、人们生存的环境与化学息息相关,下列说法中,你认为正确的是 ( )
A.汽车尾气中含有能污染空气的氮的氧化物,原因是汽油燃烧不充分
B.酸雨的形成主要是因为森林的过度采伐
C.清晨,日出后的密林中可看到缕缕光束,原因是清晨林间CO2的浓度较大
D.钢铁在潮湿的空气中更易生锈,是因为形成了原电池的缘故
12.(14分)A是生活中最常见的有机物,该化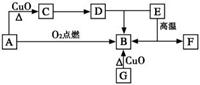
合物的蒸气对氢气的相对密度是23,是生
物燃料之一。C的溶液能发生银镜反应,
反应后的溶液经酸化可得D。G为单质,
其原子最外层电子数为次外层的2倍。F中阴阳离子个数比为1∶1,其阳离子与Ar具有相同的电子层结构,A-F的转化关系如右上图。
(1)D与E反应生成B的离子方程式:___________________________.
(2)单质G中的元素位于第________周期________族。
G与F在高温下反应生成固体H和一种还原性气体,H与H2O反应生成可燃性气体Ⅰ,Ⅰ可通过两步反应制得A。请写出:
(3)I的结构式:________________.
(4)由I制备A的两步反应的化学方程式:____________,_____________________。
(5)G与F在高温下反应生成固体H的化学反应方程式:___________。
11.(15分)盐酸、硫酸和硝酸是中学阶段常见的三种酸。请就三种酸的有关知识,回答下列问题:
(1)化学实验室制取氯化氢气体的方法之一是将浓硫酸与浓盐酸直接滴加。请在方框内补充完整用该方法制备、收集干燥氯化氢气体及尾气处理的装置简图,并在图中标明所用试剂。(固定装置不必画出)
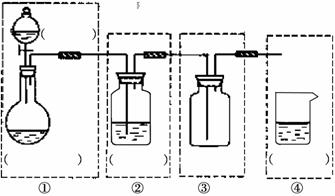
(2)在一定体积18 mol·L-1的浓硫酸中加入过量的铜片,加热使之反应,被还原的硫酸是0.9mol,则该硫酸的实际体积_________(填大于、等于或小于)100mL。
有同学提出:若使剩余的铜片继续溶解,可向其中加入硝酸盐,可行吗?_________(填“可行”或“不可行”)。
(3)将等质量的铜片分别与等体积、过量的浓硝酸和稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出可能是Cu2+浓度不同引起的,你同意这种看法吗?______(填“同意”或“不同意”),原因是_______________________。
另一同学提出溶液呈“绿色”是溶液中Cu2+与NO2共存的结果,请你设计实验探究此说法正确与否,请简述实验方案、实验现象及由此得出的结论:______________
10.(15分)下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去)。已知:(a)A、B、C为单质,且在常温常压下为气体;(b)反应①③为化工生产中的重要反应,而②为雷雨闪电时发生的反应;(c)化合物D具有漂白性,可由Cl2与NaOH(aq)反应而制得;(d)化合物H由两种元素组成,其相对分子质量为32。
请回答下列问题: 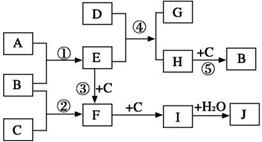
(1)反应①的条件是________,其中符合平衡移动原理的反应条件是________
(2)上述物质中,_________(填字母序号)是造成光化学烟雾的主要因素。
(3)反应③中,每有0.2molE完全反应,则电子 转移为mol。
(4)E与H的结构、性质相似,你预测H的水溶液的pH7(填:“>”、“=”或“<”),原因是___________________.用离子方程式表示)。在固态时,H为__________晶体,其沸点比E_________(填“高”或“低”)。
(5)反应⑤的化学方程式为_______________________.
9.(16分)A、B、C、D、E为原子序数依次增大的五种短周期元素,已知A的一种核素的质量数为另一种核素质量数的2倍,A和C、B和E分别位于同一主族,且B、E的质子数之和是A、C质子数之和的2倍,C、D、E这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水。试回答:
(1)写出下列元素的符号:A_______、E______。
(2)C、D、E三种元素离子半径由大到小的顺序是 _________(填相应的离子符号)。
(3)由A、B两元素形成的原子个数比为1∶1化合物的电子式是_______。
(4)C、D元素的最高价氧化物的水化物之间反应的离子方程式是:_________。
(5)用多孔石墨电极电解滴有酚酞的C元素和氯元素形成的化合物的饱和溶液,接通电源一段时间后,_______极(填电极名称)附近出现红色,另一极的电极反应式为_______,可用___________检验该电极所得产物。
8.某氯化镁溶液的密度为1.18g·cm-3,其中镁离子的质量分数为5.1%,500mL该溶液中 的物质的量浓度约等于( )
的物质的量浓度约等于( )
A.5mol·L-1
B.2.47mol·L-1
C.2.1mol·L-1
D.1.23mol·L-1
第Ⅱ卷(非选择题·60分)
7. 2008年9月份曝光的引起国人共愤的“结石宝宝”事件,与婴幼儿服用含有三聚氰胺的奶粉有关。已知三聚氰胺为白色晶体,将它用作食品添加剂可提高食品中蛋白质的检测值,俗称“蛋白精”,结构简式为
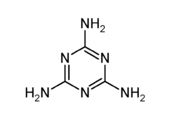
下面有关三聚氰胺说法中不正确的( )
A.三聚氰胺的化学式为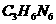
B.它在一定条件可能会与氢气发生加成反应
C.其熔点、沸点均高于三甲苯
D.假设它与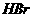 能加成,则可得到一种加成产物
能加成,则可得到一种加成产物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com