
题目列表(包括答案和解析)
4. 某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成。分四次取样品与稀硫酸反应,其实验数据记录如下表。
|
|
1 |
2 |
3 |
4 |
|
取样品质量(g) |
50.0 |
50.0 |
50.0 |
50.0 |
|
取稀硫酸质量(g) |
40.0 |
80.0 |
120.0 |
160.0 |
|
产生气体质量(g) |
0.4 |
0.8 |
1.0 |
1.0 |
试计算(1)黄铜中锌的质量分数
(2)所用稀硫酸中溶质的质量分数。
3. 某钢铁厂为了测定赤铁矿中Fe2O3的含量,将 10 g赤铁矿(杂质既不与酸反应也不溶于水)加到109.5 g10%的稀盐酸中,恰好完全反应。求:
(1)赤铁矿中Fe2O3的含量。
(2)反应后溶液中溶质的质量分数。(计算结果精确到0.1%)
2.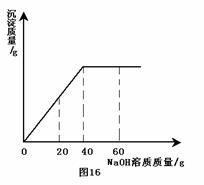 某同学在实验室发现一瓶标签残缺(如图15所示)的溶液。为了测定此溶液的溶质质量分数,他取出50g该溶液,向其中逐滴加入溶质质量分数为10%的NaOH溶液。反应过程中生成沉淀的质量与所用NaOH溶液质量的关系如图16所示。请计算此硫酸镁溶液中溶质的质量分数。
某同学在实验室发现一瓶标签残缺(如图15所示)的溶液。为了测定此溶液的溶质质量分数,他取出50g该溶液,向其中逐滴加入溶质质量分数为10%的NaOH溶液。反应过程中生成沉淀的质量与所用NaOH溶液质量的关系如图16所示。请计算此硫酸镁溶液中溶质的质量分数。
1. 化学综合实践活动小组的同学,对一造纸厂排放的污水进行检测,发现其主要的污染物为氢氧化钠。为了测定污水中氢氧化钠的含量,他们用溶质质量分数为37%、密度1.18g/cm3的浓盐酸,配得溶质质量分数为5%稀盐酸200.0g。然后取80.0g污水于烧杯中,逐滴加入这种稀盐酸至73.0g时恰好完全反应(污水中的其它成分不与盐酸反应)。请计算:
(1)配制稀盐酸时,量取了溶质质量分数为37%的浓盐酸多少毫升?
(2)污水中所含氢氧化钠的质量分数是多少?
8. )化学兴趣小组用以下装置探究炼铁的原理。
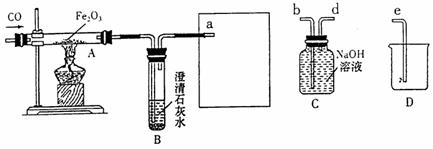
(1)加热Fe2O3之前要先通一会儿CO,目的是_________________________________。
(2)方框中连接的是C和D,导管接口的连接顺序为a→( )→( )→( ),如果导管连接错误,后果是__________________________________________。
(3)玻璃管A中发生反应的化学方程式为_________________________________,用这种方法“炼”
得的铁与工业上炼出的生铁在组成上的最大区别是_____________________________。
7. 小佳在实验室发现一种黑色粉末和一瓶标签破损的无色溶液(如图所示)。她取少量黑色粉末与溶液混合,发现立即产生了大量无色的气泡。
小佳在实验室发现一种黑色粉末和一瓶标签破损的无色溶液(如图所示)。她取少量黑色粉末与溶液混合,发现立即产生了大量无色的气泡。
(1)对这两种物质是什么,她进行大胆猜想。小佳的猜想可能是:
① 和 ;
② 和 。
(2)请你帮助小佳同学完成实验,以证明猜想①是正确的。
|
实验步骤 |
实验记录 |
实验结论 |
|
①取少量黑色粉末于试管中,滴加少量无色溶液 ② |
①有气泡产生 ② |
产生的气体是 , 原猜想①成立。 |
6. 下图是课堂中模拟炼铁的实验装置。
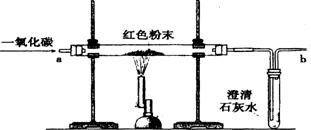
(1)写出图中标有序号的仪器名称① ,② 。
(2)实验过程中,先要进行的是_________________________ 。(填Ⅰ或Ⅱ)
Ⅰ.加热 Ⅱ.通一氧化碳
(3)A中反应的化学方程式是 。
B中反应的化学方程式是 ,B中观察到的现象是________________________。
(4)该装置的不足之处是 。
5. 某学校研究性学习小组,以一工厂生产过程中产生的废弃物“红色铁泥”为研究对象,探究红色物质的成分,请你参与他们的活动。
[小组讨论]
甲观点:红色物质是铜
乙观点:红色物质是氧化铁
丙观点:红色物质是氢氧化铁
丁观点:红色物质是氧化铁和氢氧化铁的混合物
[查阅资料]
该厂“红色铁泥”主要是生产过程中使用铁触媒(一种催化剂)后的废弃物,除红色物质外,还含有通常不与酸、碱和氧气反应的物质。氢氧化铁受热易分解
[提出假设]
乙、丙、丁三种观点存在合理性
[实验验证]
Ⅰ 取适量“红色铁泥”晒干,称量其质量为m1g
Ⅱ 将“红色铁泥”置于坩埚中充分加热并在干燥器中冷却后,称量其质量为m2g
请回答下列问题:
⑴当m1=m2时,则红色物质为 。
⑵当m1>m2>160m1/214时,则“红色铁泥”中一定含有氧化铁吗? (填写“一定”或“不一定”),理由是 。
⑶假定“红色铁泥”中“红色物质是氢氧化铁”,请写出回收“红色铁泥”中的铁元素制得“铁红”(化学式为Fe2O3,是红色油漆的重要原料)过程中的化学方程式:
①
② ;③ 。
4. 小明在学习金属活动性顺序时,对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”这句话产生了好奇。为什么用“一般’’这个词呢?难道还有例外吗?
[查阅资料]Na性质活泼,常温下,与氧气反应,也可以与水反应放出氢气。
[实验与分析]①在实验室中,金属钠保存在煤油中;②用镊子从煤油中取出金属钠,放在滤纸上,用小刀切下一小块,投人蒸馏水中,发现钠块立刻熔化成银白色小球,在水面上到处游动,滴入酚酞试液后溶液变成红色;③往硫酸铜溶液中,投入一小块钠,又出现蓝色沉淀,但没有红色物质析出。
(1)金属钠保存在煤油中的原因_________________________
(2)从实验②中,你能得出哪些信息?(任写三条)。________;_____________;____________.
(3)写出钠与硫酸铜溶液反应的化学方程式_______________;__________________
[结论]活动性较强的金属不一定将位于其后面的金属从它们的盐溶液中置换出来。
3. 小明在做某次实验时,发现一瓶瓶口已敞开不知多久的氢氧化钠溶液(下称试液)。联想到药品保存注意事项,小明利用提供的试剂(CaCl2溶液、盐酸、CaCO3固体、酚酞)对试液是否变质展开了探究。
他首先的猜想是:试液没有变质,溶液的溶质还是NaOH。
小明通过查资料知Na2CO3呈碱性。他根据首先的实验方案进行的实验是:取少量试液加入试管,滴入酚酞,观察到试液变红。由此得出的结论是原试液没有变质,还是NaOH。
①小明反思实验验证,觉得不够完善,理由是
②完善实验方案后,他从提供的试剂中选取一种试剂进行实验发现原试液确已变质。请你写出他这次实验的操作、现象
小明是个爱思考的学生,他又有一个新的疑问:试液真是没有NaOH了吗?他又作了探究:
③猜想:
④实验验证:(要求写出操作、现象)
,试液中还有NaOH。
⑤通过上述探究,小明明白了:氢氧化钠溶液暴露在空气中会变质,故应 保存。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com