
题目列表(包括答案和解析)
24.TOC向pH=6的蒸馏水中加入一定量的NaHSO4晶体,保持温度不变,测得溶液的
pH=2,下列有关叙述中不正确的是( )
A.T>25℃ B.由水电离出来的c(H+)=1×10-10mol/L
C.c(H+)=c(OH-)+c(SO42-) D.加入NaHSO4后水的电离程度增大
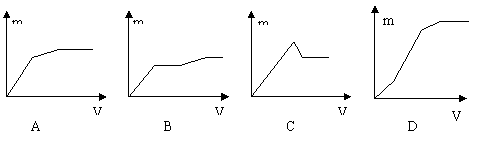
23、向用盐酸酸化的MgSO4溶液中加入Ba(OH) 2溶液,产生的沉淀量m与加入的体积V之间的关系,不可能是下图中的( )
22、下列实验操作会引起测定或配制结果一定偏高的是( )
A.测定硫酸铜晶体中结晶水含量的实验中,晶体加热完全失去结晶水后,将盛试样的坩埚放在实验桌上自行冷却
B.中和滴定用的锥形瓶中加入待测液后,再加少量蒸馏水稀释
C.中和热测定实验中,用铜丝代替玻璃搅拌棒(只比较数值的大小)
D.配制一定物质的量浓度的溶液,定容时俯视。
21.X、Y、Z和R为原子序数依次递增的四种元素。其中X、Y同周期,X的最高正价是最低负价绝对值的3倍,Y、Z、R同主族,R为人体所需的微量元素。下列说法不正确的是
A.127R-的核外含有54个电子
B.Y、Z、R的氢化物溶于水后的的酸性逐渐减弱
C.有l molY的单质与水发生反应则转移电子的物质的量为2 mol
D.在含有Z单质的水溶液中,通入足量XO2气体,则溶液由黄色变为无色
20.某无色溶液中,若加入NaClO溶液或适量HCl溶液,均能产生淡黄色沉淀。则该溶液中可能大量存在的离子组是:
A.Na+、K+、S2-、Cl- B.H+、Na+、S2-、NO3-
C.K+、Ca2+、S2-、SO32- D.Na+、S2-、SO32-、SO42-
19、某化学课外活动小组甲同学欲制备收集A气体,乙同学欲制备收集B气体(制备方法、装置、试剂的化学式均相同)。甲采用排水法却收集到B气体,乙用排空气法却得A气体。下列关于A、B两种气体的叙述不正确的是
A、 B气体只能通过人工合成 B、 A、B气体分子中均含有极性共价键
C、 A、B均不属于酸酐 D、 A、B气体相对分子质量之差为16
18.向1.00 L 0.3 mol/L的NaOH溶液中缓慢通入CO2气体至溶液增重8.8g,所得溶液中
A.溶质为Na2CO3 B. 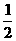 c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C、溶质为Na2CO3、NaHCO3 D.c(Na+)=c(HCO3-)+2c(CO32-)+c(OH-)-c(H +)
17.研究性学习小组做铜与浓硫酸反应实验时,发现试管底部有白色固体并夹杂有少量黑色物质。倒去试管中的浓硫酸,将剩余固体(含少量浓硫酸)倒入盛有少量水的烧杯中,发现所得溶液为蓝色,黑色固体未溶解。过滤、洗涤后,向黑色固体中加入过量浓硝酸,黑色固体溶解,溶液呈蓝色,所得溶液加BaCl2溶液后有白色沉淀生成。下列所得结论正确的是
A.铜与浓硫酸反应所得白色固体是CuSO4
B.加BaCl2溶液后所得白色沉淀是BaSO3
C.白色固体中夹杂的少量黑色物质可能是CuO
D.白色固体中夹杂的少量黑色物质中含元素Cu、S
16、元素A和元素B的原子序数都小于18。已知A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M电子层电子数为(a-b),L电子层电子数为(a+b),则A、B两元素所形成的化合物的性质和用途可能有:
A、属于离子化合物; B、一定条件下能与碳酸钠反应
C、能与水反应生成酸; D、可用于制造光导纤维
15、下列各组物质中,不能按 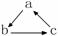 (“→”表示一步完成)关系相互转化的是( )
(“→”表示一步完成)关系相互转化的是( )
|
选项 |
A |
B |
C |
D |
|
a |
NaOH |
HNO3 |
HCl |
S |
|
b |
Na2CO3 |
NO |
Cl2 |
SO3 |
|
c |
NaCl |
NO2 |
HClO |
H2SO4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com