
题目列表(包括答案和解析)
36、(6分)有NaCl和NaNO3的混合物20克,完全溶于水后,向溶液中滴加136克的AgNO3溶液恰好完全反应,有沉淀生成,将沉淀滤出洗涤烘干,干燥后质量为28.7克。求:
(1)原混合物中NaCl的质量分数;
(2)反应后,滤液中溶质的质量分数是多少?
35.(5分)在科学家的眼里二氧化碳是可以利用的重要资源,只要有合适的条件,可以像发生光合作用那样将二氧化碳转变为所需要的产物。我国科学家陈乾旺等研究成果表明,在440℃和800个大气压条件下,二氧化碳和金属钠反应产生金刚石和碳酸钠,合成的金刚石直径最大可达1.2毫米,完全可以满足工业用途。
(1)二氧化碳与金属钠反应生成金刚石和碳酸钠的化学方程式为: ,
(2)理论上66克二氧化碳可以制得多少克金刚石?
34.在研讨酸、碱、盐相互间反应关系时,甲、乙两组同学利用碳酸钠溶液按照以下步骤完成实验(假设每步反应都完全)。
 第一步:向碳酸钠溶液中加试剂X,过滤,得白色沉淀;
第一步:向碳酸钠溶液中加试剂X,过滤,得白色沉淀;
第二步:向该沉淀中加试剂Y,沉淀全部溶解,有气体生成,得无色溶液;
第三步:向该溶液中加试剂Z,过滤,最终得不溶于酸的白色沉淀和硝酸镁溶液。
(1)甲、乙两组同学共进行三次实验,其中所选的试剂均不相同,乙组同学最终得到的不溶于酸的白色沉淀不同于甲组。请下表空格中填入相关的化学式:
|
|
试剂X |
试剂Y |
试剂Z |
最终得到的白色沉淀 |
|
|
甲组 |
① |
MgCl2 |
HCl |
AgNO3 |
AgCl |
|
乙组 |
② |
BaCl2[或Ba(OH)2] |
HNO3 |
MgSO4 |
▲ |
|
③ |
▲ |
▲ |
▲ |
(2)请写出乙组实验③中碳酸钠溶液与试剂X反应的化学方程式:
▲
33.工业上是用氨气还原氧化铜制取铜的。某校化学兴趣小组为探究该反应能否进行并验证其生成物,查阅了大量资料并设计了一系列实验。查阅到的信息:
|
(2)氨气还原氧化铜制取铜的反应原理:2NH3+3CuO===3Cu+N2+3H2O
某小组设计了如下实验装置并进行实验:
氯化铵和熟石灰 氢氧化钠固体

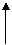
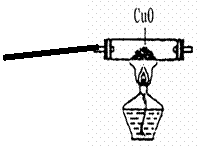

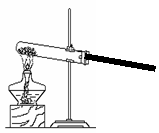
试回答:
(1)写出装置A中试管内发生反应的化学方程式:▲ ;
(2)装置B所起的作用是 ▲ ;
(3)装置C中可观察到的实验现象是 ▲ ;
(4)你认为该小组的实验设计还存在着哪些不足? ▲
32、实验室用过氧化氢(H2O2)制取氧气时常用二氧化锰作催化剂。有同学提出硫酸铜能否代替二氧化锰作该反应的催化剂。下面请你一起参与实验探究,并回答问题:
(1)作出假设:硫酸铜可以作过氧化氢分解反应的催化剂。
(2)实验探究:
实验1:取甲、乙两支试管,分别加入等体积的5%过氧化氢溶液。在甲试管中加入适量的硫酸铜溶液,发现甲试管中迅速产生气泡,在乙试管中加入适量的蒸馏水,观察不到气泡产生。
实验2:取适量实验1中甲试管反应后的溶液,分别装入丙、丁试管中。向丙试管内滴加BaCl2溶液,有白色沉淀产生;向丁试管内滴加NaOH溶液,有蓝色絮状沉淀产生。
(3)分析讨论:
①实验1中设置乙试管起 ▲ 作用。
②实验2中向丙试管内滴加BaCl2溶液产生白色沉淀的化学方程式是 ▲ 。
31、维生素C主要存在于蔬菜和水果中,它能促进人体生长发育,增强对疾病的抵抗力。目前药店里有一种“维C泡腾片“的药品能补充人体维生素C的需求。一次小明看到爷爷冲饮这种药品的过程:在一杯温开水中放入一片该药品,药品迅速溶解,同时出现了大量的气泡。小明对这一现象产生了浓厚的兴趣,于是他向爷爷要了几片这种”维C泡腾片“在家中进行实验:在盛有温水的杯中加入该药品,并用燃着的火柴伸到杯口,发现火柴熄灭,由此小明初步推测了该气体中含有的成分,但还不能最终确定。
为了进一步确定自己的推测,第二天小明带着药品去学校实验室做了如下实验:
|
操作 |
感觉气体的色、味 |
气体通入紫色石蕊试液 |
气体通入澄清石灰水 |
|
现象 |
无色、无味 |
紫色石蕊试液变红色 |
澄清石灰水变浑浊 |
(1)分析小明的实验现象,可以确定该气体中一定有 ▲ 。
(2)从该“维C泡腾片”说明书的注意事项中,小明还发现了这样的叙述:冲饮时水温不能高于80oC;冲后即服用。从中你可以推测维生素C还有哪些性质? ▲。(写出一项即可)
30、小婧同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液滴加稀盐酸一会儿后,又发现忘记了滴加指示剂,因而无法确定盐酸与氢氧化钠是否恰好完全反应。为了证明这两种物质是否恰好完全反应,小婧从烧杯中取了少量反应后的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色。于是她得出“两种物质已恰好完全中和”的结论。
(1)你认为她得出的结论是否正确 ;
(2)写出该中和反应的化学方程式 ;
(3)请你另设计一个实验,探究上述烧杯中的溶液是否恰好完全中和,填写下表:
|
实验方法 |
可能观察到的现象 |
结论 |
|
▲ |
▲ |
中和完,盐酸过量 |
29、以锌粒、氧化铜、稀硫酸为原料,用两种不同的方法制取铜,写出化学反应方程式。
(1) ▲ ▲ ;
(2) ▲ ▲ 。
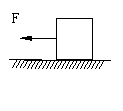
28.如图所示,用水平力F拉着重为100N的物体,在水平地面上向左匀速移动了5m,物体所受地面的摩擦力大小为20N,则拉力做功_____▲____,重力做功
___▲__。
27.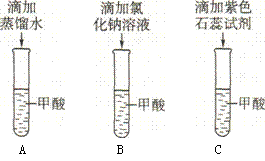 甲酸是一种无色、有刺激性气味的液体,有较强的腐蚀性。小明想知道甲酸是否具有酸性,做了如下探究:
甲酸是一种无色、有刺激性气味的液体,有较强的腐蚀性。小明想知道甲酸是否具有酸性,做了如下探究:
(1)他作出的猜想是“甲酸具有酸性”。你认为下列哪一项实验设计能够检验这一猜想?请用图中字母表示___▲__。
(2)若小明的猜想是正确的,则甲酸就会像盐酸那样,能与碳酸钠反应,产生______▲__气体。
 (3)甲酸(HCOOH)是有机物,浓硫酸能将有机物中的氢元素和氧元素“脱出”结合成水。利用浓硫酸的脱水性,实验室里将甲酸和浓硫酸混合加热进行反应,该反应中甲酸脱水后会转变成_____▲____ 。
(3)甲酸(HCOOH)是有机物,浓硫酸能将有机物中的氢元素和氧元素“脱出”结合成水。利用浓硫酸的脱水性,实验室里将甲酸和浓硫酸混合加热进行反应,该反应中甲酸脱水后会转变成_____▲____ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com