
题目列表(包括答案和解析)
2、60克碳酸钠溶液和20%的盐酸(密度为1.1克/厘米3)完全反应后,全部转化为氯化钠,溶液的质量减小了4.4克。求:
(1)消耗20%的盐酸多少毫升?
(2)反应后溶液中溶质的质量分数是多少?
1、取未知浓度的盐酸10克,加入足量的硝酸银溶液,反应后生成5.74克氯化银沉淀,求:
(1)该酸的溶质质量分数为多少?
(2)把200克这种盐酸稀释为质量分数为10%的盐酸,需加水多少克?
8、某工厂的废水中含2%的H2SO4,可采用边排边中和的方法处理至中性。排放及处理的方法如下图:
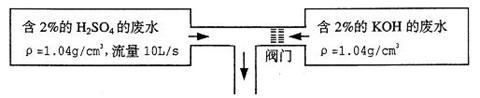
(1)当流量阀门调至某一位置时,处理后的废水可使紫色石蕊试液变红,此时应将流量阀门调 (填“大”或“小”)才能使处理后的废水呈中性。
(2)应使含2%的KOH废水的流量为 L/s,才能使处理后的废水pH=7。
(保留二位小数)
7、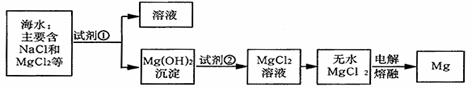 镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。主要步骤如下:
镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。主要步骤如下:
(1)为了使MgCl2转化为Mg(OH)2,试剂①可以选用 ,要使MgCl2完全转化为沉淀,加入试剂①的量应 。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 。
(3)试剂②可以选用 。
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,写出该反应的化学方程式 。
6、某同学设计了分离NaCl和CaCl2两种固体的实验方案:

据此回答问题:
(1) 物质B是______________________,试剂甲是________________。
(2) 根据以上方案得到的NaCl固体经测定含有杂质,该杂质是___________。要得到较纯净的NaCl固体,以上方案应作如何改进?________________________ ____________。
5、实验室里,用氯化铵晶体跟氢氧化钙粉末混合加热制取氨气。它是一种无色的,有刺激性气味
的,密度比空气小,而溶于水且能跟水反应生成氨水的气体,制取氨气过程中还有氯化钙和水生成。
(1)写出制取氨气的化学方程式:
(2)实验室制取(不包括收集)氨气的装置,可选用制取 (H2或O2或CO2)的装置。其理由是 。收集氨气可用 法。
4、据报道,我国将推广“车用乙醇汽油”技术。乙醇(化学式为C2H5OH)完全燃烧时,生成CO2和H2O;乙醇燃烧时如果氧气不足,还有CO生成。现有下列装置(如图所示):
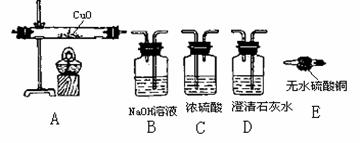 ⑴试用上述装置设计一实验,验证乙醇不完全燃烧的产物中含有CO、CO2、H2O 3种气体。应
⑴试用上述装置设计一实验,验证乙醇不完全燃烧的产物中含有CO、CO2、H2O 3种气体。应
将乙醇燃烧的产物依次通过(填写装置的序号)_____________________________,最后进行尾气处理,其中装置A反应的化学方程式是___________________________,装置C的作用是____________________,装置E的作用是_____________________。
⑵若乙醇燃烧的产物中,水的质量是24.3克,则参加反应的乙醇的质量是________。
1、钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注,常温下钛不能和非金属、强酸反应,红热时却可与许多常见的非金属单质反应,钛是航空、宇航、军工、电力等方面的必需原料。地壳中含钛矿石称金红石(TiO2),目前大规模生产的方法是:
第一步:金红石、碳粉混合物在高温条件下能入氯气制得TiCl4和一种可燃性气体,该步发生反应的化学方程式是______________________,该反应的还原剂是__________。
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛,该步反应的化学方程式是______________________________。
|
⑴木材干馏木精属于______________变化。
⑵甲醇是无色透明、易挥发的液体,这是它的________________性质。
⑶写出生产甲醇的化学方程式__________ _______。
⑷推断甲醛的化学式M应为_________ __________。
20、只需用水就能直接鉴别的一组物质是( )
A、Na2SO4 CuSO4 CaCO3 B、AgCl BaSO4 CuSO4
C、NaCl CaCl2 BaCl2 D、BaCl2 AgCl Na2CO3
二、简答题
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com