
题目列表(包括答案和解析)
6.下列关于元素周期表和元素周期律的说法不正确的是
A.从氟到碘,生成的氢化物熔沸点逐渐升高,稳定性逐渐减弱
B.因为钠原子比铝原子容易失去电子,所以钠比铝的还原性强
C.从钠到氯,最高价氧化物的水化物碱性逐渐减弱,酸性逐渐增强
D.氧与硫为同主族元素,氧比硫的原子半径小,氧比硫的氧化性强
5. 在一定温度下的定容器中,当下列物理量不再变化时,表时反应A(g)+2B(g) C(g)+D(g)已达到平衡状态的是
在一定温度下的定容器中,当下列物理量不再变化时,表时反应A(g)+2B(g) C(g)+D(g)已达到平衡状态的是
① 混合气体的压强 ② 混合气体的密度
③ B的物质的量浓度 ④ 混合气体总物质的量
⑤ 混合气体的平均相对分子质量 ⑥ v(A)正=2v(B)逆
⑦ 混合气体的总质量 ⑧ 混合气体总体积
A.①③④⑤ B.①②③④⑤⑦
C.①③④⑤⑧ D.①②③④⑤⑥⑦⑧
4.下列有关说法正确的是
A.物质熔沸点的高低顺序是:晶体硅>氯化钠>冰>氖气
B.微粒半径由小到大顺序是:H-<Li+<H+
C.溶液中结合H+能力由强到弱的顺序是:SO2-4>H2PO-4>CH3COO->HCO-3
D.CO2、HClO、CF4、PCl3四种物质分子中所有原大都满足最外层为8电子的稳定结构
3.下列说法正确的是
A.明矾净水过程中不涉及化学变化
B.由同种元素组成的物质一定是纯净物
C.风化、石油分馏和碘的升华都是物理变化
D.在化学反应中,反应前后原子种类、数目和质量一定不变
2.探测冥王星(Pluto)的“新地平线(New Horizons)”号具有10.9kg钚-238(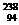 Pu)燃料的核电池系统,核电池是由辐射β射线(高速电流)的放射源,收集这些电子的集电器,以及两者之间的绝缘体三部分组成。下列有关说法正确的是
Pu)燃料的核电池系统,核电池是由辐射β射线(高速电流)的放射源,收集这些电子的集电器,以及两者之间的绝缘体三部分组成。下列有关说法正确的是
A.钚电池是将核能转化为电能
B.核燃料是可再生能源
C.放射源一端为正极,集电器一端为负极
D.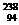 Pu的原子质量是12C原子质量的238倍
Pu的原子质量是12C原子质量的238倍
1.2003年,IUPAC(国际纯粹与应用化学联合会)推荐原子序数为110的元素的符号为Ds,以纪念该元素的发现地(Darmstadt,德国)。下列关于Ds的说法不正确的是
A.Ds原子的电子层数为7 B.Ds是超铀元素
C.Ds原子的质量数为110 D.Ds为金属元素
23.(7分)硝酸是重要的化工原料。在硝酸工业生产中产生的尾气可用纯碱溶液吸收,有关的化学反应有(①式不完整,未配平);
NO2+NaCO3=NaNO2+ +CO2①
NO+NO2+Na2CO3=2NaNO2+CO2②
请按要求回答下列问题:
(1)①式中缺少的产物化学式为 ,其中氧化剂与还原剂物质的量之比为 。
(2)配制1000g质量分数为21.2%的纯碱吸收液,需n(Na2CO3·10H2O)为 。
(3)现有1000g质量分数为21.2%的纯碱吸收液,在20℃用于吸收硝酸厂工业尾气。已知当产生22.4L(标准状况)CO2时,吸收液质量增加44g,求此时溶液中主要阴离子物质的量之比约为 。
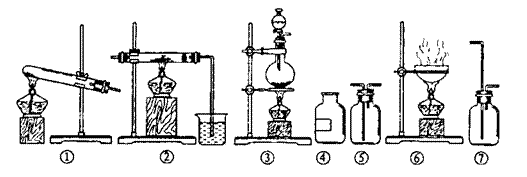
22.(17分)欲制无水氯化铝并保存备用。现有仪器如下图所示,并有食盐晶体、水、固体烧碱、铝粉、二氧化锰、浓硫酸等六种试剂。请回答下列问题:
 (1)设计的制取思路是:
→
→
(1)设计的制取思路是:
→
→
(2)从上列仪器中选取必须的几种,连接成一个制无水氯化铝的连续装置,按前后顺序填写图的编号(不一定填满)。
仪器编号: 、 、 、 、 ;
放入试剂: 、 、 、 、 。
(3)该实验中装置有不足之处,请指出
21.(10分)某校研究性学习小组设计了如图所示装置进行
有关实验,实验时将分液漏斗中A逐滴加入烧瓶B中。
(图中铁架台、铁夹已略去,要求填写的试剂均填化学式)
(1)若A为浓硫酸,B为第三周期金属元素的单质,其在常温下难与水反应;C为品红溶液,实验观察到C中溶液腿色,则B ,若使C试管溶液恢复原来的颜色,可采取的操作为 。
(2)若B为块状大理石,C为饱和Na2CO3溶液,实验中观察到C试管内溶液变浑浊,则C试管中发和反应的离子方程式为 。
(3)若B是生石灰,实验中观察到C溶液中先形成沉淀,而后沉淀溶解,当溶液恰好澄清时,关闭E,然后将C放入盛有沸水的烧杯中,静置片刻,观察到试管壁上出现光亮银镜。则A是 ,C是 与葡萄糖的混合液。仪器D在此实验中的作用是 。写出B中发生反应的方程式 。
20.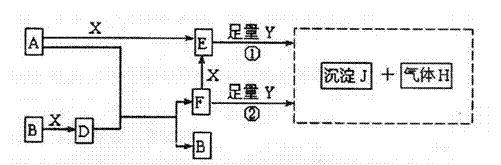 (14分)下图所示反应有直接进行的,也有在溶液中进行的,其中部分产物已略去。已知:A是固体单质;B、X、H为气体单质;D属于可溶于水的强电解质,一个D分子中含有18个电子,Y为淡黄色固体。
(14分)下图所示反应有直接进行的,也有在溶液中进行的,其中部分产物已略去。已知:A是固体单质;B、X、H为气体单质;D属于可溶于水的强电解质,一个D分子中含有18个电子,Y为淡黄色固体。
(1)化学式:B为 ,F为 。
(2)用电子式表示D的形成过程为 。
(3)A是一种非常重要的工业产品。据统计,地球上每年由于腐蚀而消耗的A约占A年产量的10%。A发生腐蚀的主要原因是(填写下同的选项序号) ;
a.直接与氧气发生化学腐蚀 b.通过原电池反应发生腐蚀 c.因溶于水而消耗掉。
若你选定选项a或c,请写出相应的化学方程式;若你选定选项b,请写出正极的电极反应式:
(4)已知H为无色,密度比空气大的气体,则①中所涉及的反应的化学方程式为,
(5)写出F 水溶液与足量Y反应的离子方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com