
题目列表(包括答案和解析)
4.手机是人们常用的通讯工具,它传递信息依靠的是
A.电磁波 B.红外线 C.超声波 D. 次声波
3.太阳是一个由炽热气体组成的球体,太阳大气层从里到外可分为3层,依次是
A.日核、光球层、色球层 B.光球层、色球层、日冕层
C.太阳黑子、色球层、日冕层 D.太阳黑子、耀斑、色球层
2.下图是某些物品的近似pH,呈碱性的是

1.植物类群中最复杂、最高等的是
A.苔藓植物 B.被子植物 C.蕨类植物 D.藻类植物
38.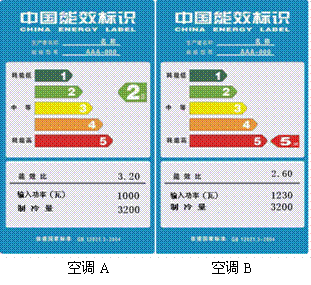 我国对家用电冰箱、空调这两个产品率先实施能源效率标识制度,以后生产、销售、进口的空调、冰箱均应在显著位置粘贴“中国能效标识”的标签,如图所示。能效标识将能效分为1、2、3、4、5五个等级,等级1表示产品最节能,等级5是市场准入指标,低于该等级要求的产品不允许生产和销售。
我国对家用电冰箱、空调这两个产品率先实施能源效率标识制度,以后生产、销售、进口的空调、冰箱均应在显著位置粘贴“中国能效标识”的标签,如图所示。能效标识将能效分为1、2、3、4、5五个等级,等级1表示产品最节能,等级5是市场准入指标,低于该等级要求的产品不允许生产和销售。
(1)图中所示的是两台空调的能效标识,按照图中所给的输入功率,试计算空调A在220V电压下工作时的电流是多少安培?(计算结果保留两位小数)
(2)两台空调的制冷量相同,但能效比却不相 同。假设两台空调的使用寿命都为12年,平均每台每年使用500小时,试求出使用12年,高效节能空调A比一般节能空调B能节约多少千瓦时的电能?
37.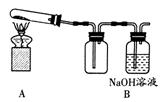 某课外活动小组的同学将16克氧化铜和过量的炭粉均匀混合,用下图所示装置进行实验。图中铁架台等装置已略去。请回答有关问题:
某课外活动小组的同学将16克氧化铜和过量的炭粉均匀混合,用下图所示装置进行实验。图中铁架台等装置已略去。请回答有关问题:
(1)实验中最多能得到铜多少克?(写出计算过程)
(2)同学们想通过测定消耗碳、氧元素的质量和生成二氧化碳的质量,以进一步分析氧化铜和炭粉反应产生的气体除CO2外是否还有其它产物。反应一段时间后停止加热,冷却到室温。反应前、后测得的数据如下:
|
装置 |
反应前 |
反应后 |
|
A |
试管的质量36.2 克 氧化铜和炭粉混合物的质量20.0克 |
试管和固体物质的质量54.8 克 |
|
B |
反应后瓶内液体比反应前增重1.1 克 |


分析数据发现,反应中消耗碳和氧元素的质量 ▲ (填“大于”或“小于”或“等于”)生成二氧化碳的质量。下列4项中跟这一结果有关的有哪几项? ▲ 。(填编号)
A.装置中还有一部分CO2未被NaOH溶液吸收
B.氧化铜和炭粉反应产生的气体除CO2外还有CO
C.氧化铜和炭粉没有完全反应
D.该反应不符合质量守恒定律
(3)有同学认为用图示装置C代替上面的装置A,加热前先通一会气体X,停止加热后再通一会该气体,这样可使实验测得的数据更能准确的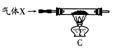 说明问题。你认为在O2、N2和H2三种气体中,
说明问题。你认为在O2、N2和H2三种气体中,
X应选择哪一种气体? ▲ 。
36.站在教学楼前水泥地上的九年级同学小刚的质量为48千克,正准备走上6米高的三楼试场参加科学考试,如果小刚双脚站立时与地面的接触面积是0.04米2,走上三楼试场的时间为24秒(g取10N/Kg)求:
(1)小刚站在教学楼前水泥地上时对水泥地的压强为多少?
(2)小刚走上三楼试场的过程中,他做功的功率是多少?
35.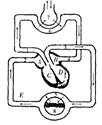 如图是人体气体交换与血液循环的关系模式图(图中7表示肺泡,8表示组织细胞),请据图并结合所学知识分析解答下列问题:
如图是人体气体交换与血液循环的关系模式图(图中7表示肺泡,8表示组织细胞),请据图并结合所学知识分析解答下列问题:
(1)在心脏的A与C之间、B与D之间有防止血液倒流的 ▲ 。
(2)图中[6]与[7]之间的气体交换过程称为肺泡内的气体交换,它是通过气体的扩
散作用来实现的。其中二氧化碳的扩散方向是[6] ▲ [7]。(用箭头表示扩散方向)
(3)图中[8]内的气体与[5]内血液中的气体交换后,从血管E处流出的是 ▲ 血。
34.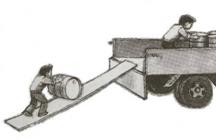 小强看到在没有起重机的情况下,工人要将油桶搬运上汽车,常常用如图所示的方法。小强想:为什么不直接将油桶抬上车呢?难道这样做可以省力吗?小强带着疑问去查阅有关资料后了解到:用斜面搬运同一物体时的推力大小跟斜面长度、斜面高度、斜面粗糙程度等因素有关。小强根据以上查阅的资料提出了一个探究的问题:沿斜面推力的大小与斜面的长度有什么关系?
小强看到在没有起重机的情况下,工人要将油桶搬运上汽车,常常用如图所示的方法。小强想:为什么不直接将油桶抬上车呢?难道这样做可以省力吗?小强带着疑问去查阅有关资料后了解到:用斜面搬运同一物体时的推力大小跟斜面长度、斜面高度、斜面粗糙程度等因素有关。小强根据以上查阅的资料提出了一个探究的问题:沿斜面推力的大小与斜面的长度有什么关系?
(1)你认为小强探究搬运同一物体时沿斜面推力的大小与斜面长度的关系时,应控制的变量有 ▲ 。
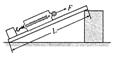 (2)小强选用了一把弹簧秤、一块8N的长方体重物、五块长度不同的由同种材料做成的光滑木板,按如下图所示进行了实验,实验时控制斜面高度为 0.2m不变。实验测得的数据如下表所示:
(2)小强选用了一把弹簧秤、一块8N的长方体重物、五块长度不同的由同种材料做成的光滑木板,按如下图所示进行了实验,实验时控制斜面高度为 0.2m不变。实验测得的数据如下表所示:
|
次数 |
物重G/N |
斜面高h/m |
弹簧称示数F/N |
斜面长L/m |
|
1 |
8 |
0.2 |
4.0 |
0.4 |
|
2 |
8 |
0.2 |
2.0 |
0.8 |
|
3 |
8 |
0.2 |
1.6 |
1.0 |
|
4 |
8 |
0.2 |
1.0 |
1.6 |
|
5 |
8 |
0.2 |
0.8 |
2.0 |
分析实验数据,小强得到的结论是: ▲ 。
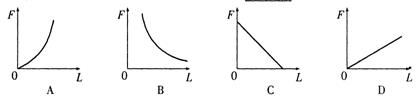
(3)下列四个图中,你认为哪个图能正确表示F与L的关系? ▲ 。
33.同学们都有这样的学习、生活经验:木炭在氧气中燃烧比空气中燃烧得更旺;夏天,将食品放在冰箱里不容易腐烂。说明反应物的浓度和温度对化学反应快慢(反应速率)有影响。那么,浓度和温度是如何影响化学反应速率的?
(1)提出假设:a.浓度越大,化学反应越快;b.温度越高,化学反应越快。
(2)设计方案:同学们利用铁粉和盐酸反应来探究上述问题,设计了下列3组实验。
|
组别 |
温度/℃ |
铁粉质量/g |
盐酸的质量分数和体积 |
观察气泡产生的速率 |
|
1 |
10 |
2.8 |
10%、50 mL |
|
|
2 |
10 |
2.8 |
20%、50 mL |
|
|
3 |
20 |
2.8 |
10%、50 mL |
|
(3)分析探究:将铁粉加入到盛盐酸的烧杯中发生反应,写出反应的化学方程式 ▲ 。
哪两组实验用来探究“温度越高,化学反应越快”的假设? ▲ 。
(4)讨论反思:事实上,化学反应的发生,是反应物的微观粒子相互接触、碰撞的结果。请你解释“盐酸浓度越大,与铁粉反应越快”的原因 ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com