
题目列表(包括答案和解析)
1.2007年9月,美国科学家宣称:普通盐水在无线电波照射下可燃烧,这伟大的发现,有望解决用水作人类能源的重大问题。无线电频率可以降低盐水中所含元素之间的“结合力”,释放出氢原子,若点火,氢原子就会在该种频率下持续燃烧。上述中“结合力”实质是
A.分子间作用力 B.氢键 C.非极性共价键 D.极性共价键
22. (10分)某钠盐溶液可能含有阴离子NO3-、CO32-、SO32-、SO42-、Cl-、Br-、I-、为鉴别这些离子,分别取少量溶液进行以下实验:
①测得混合液呈碱性;
②加HCl后,生成无色无味气体,该气体能使饱和石灰水溶液变浑浊;
③加CCl4后,滴加少量氯水,振荡后,CCl4后层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3,溶液中析出白色沉淀。
分析上述5个实验,写出每一步实验鉴定离子的结论与理由。
实验① ;
实验② ;
实验③ ;
实验④ ;
实验⑤ ;
21.(6分)在一个容积固定不变的密闭容器中进行反应:2A(g)+B(g)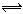 3C(g)+D(s),已知将2molA和1molB充入该容器中,反应在某温度下达到平衡时,C的物质的量为Wmol,C在平衡混合气体中的体积分数为n%。
3C(g)+D(s),已知将2molA和1molB充入该容器中,反应在某温度下达到平衡时,C的物质的量为Wmol,C在平衡混合气体中的体积分数为n%。
(1) 如果用下列情况的配比作起始物,在同样的容器和温度下达到平衡,其结果一定是:C的物质的量为2Wmol,C在平衡混合气体中的体积分数仍为n%的是
A.4molA+2molB B.6molC+1molD C.1molA+0.5molB+1.5molC+0.5molD
D.2molA+1molB+3molC+1molD E.2molA+1molB+3molC+2molD
(2) 若维持该题条件不变,仅从生成物开始配比,要求达到平衡时,C的物质的量仍为Wmol,则D的起始物质的量n(D)应满足的条件是 (用含W的代数式表示)
20. (6分)A、B、C、D、E、F是中学化学常见的6种物质,它们之间有如下转化关系。其中,B、D在通常情况下是气体物质,F溶液呈碱性,E溶液是AgNO3,C是白色沉淀。试回答:
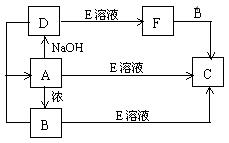
(1) C的化学式为 ,D的电子式为 。
(2) 写出D+E ® F的离子方程式: 。
0.5molN2、1.5molH2 。此时VA=2VB 。维持温度不变,
A、B中的反应均达到平衡。平衡时,两容器中反应放
出的热量分别为QAkJ、QBkJ,A容器中气体体积为起
始时的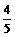 。(1)平衡时A容器中NH3的体积分数是
。
。(1)平衡时A容器中NH3的体积分数是
。
平衡时B容器中压强与A容器中压强之比 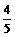 (填>、< 或=)。
(填>、< 或=)。
(2)已知在该温度下:N2(g)+3H2(g)=2NH3(g) △H=–Q kJ/mol。试确定QA、2QB、Q三者大小关系:
(3)若保持温度不变,向A容器中补加2molHe,向B容器中补加0.5molN2、1.5molH2,再次达到平衡时,A容器中N2的转化率______________(变大,变小,不变),B容器中N2的转化率______________(变大,变小,不变)。
19. (10分) 有A、B两个容器,A为恒压容器,B为恒容容器。
 在相同温度下A中充入1molN2、3molH2,B中充入
在相同温度下A中充入1molN2、3molH2,B中充入
(1)在A、B、D、E四种元素的最简单氢化物中,沸点最高的是
____(填化学式),由D、E两种元素组成的化合物属于
晶体。
(2)A、B、D、M可组成多种18电子分子,其中两种的结构可分别表示为M2B-BM2和AM3-BM2,请根据这两种分子的结构特点再写出2种具有18电子的有机物的结构简式(用元素符号表示)______________________、_________________________。

18. (12分)硫酸铵是一种常用的铵态氮肥。下表是硫酸铵化肥品质的主要指标。

|
项目 |
指
标 |
||
|
优等品 |
一等品 |
合格品 |
|
|
外观 |
白色晶体,无可见机械杂质 |
无可见机械杂质 |
|
|
氮(N)含量 |
≥21.0% |
≥21.0% |
≥20.5% |

新华中学化学研究性学习小组为本地农业生产服务,对某农用品商店出售的一等品硫酸铵化肥的品质进行探究。
[观察外观]该硫酸铵化肥无可见机械杂质。
[实验探究]按右图所示装置进行实验。
(1)烧瓶内发生反应的离子方程式为:

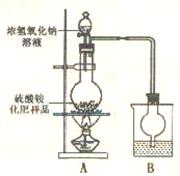 烧杯中最适宜盛放的试剂是
(填“浓硫酸”、“稀硫酸”或“水”)。
烧杯中最适宜盛放的试剂是
(填“浓硫酸”、“稀硫酸”或“水”)。
(2)实验过程中,需往烧瓶中加入足量浓氢氧化钠溶液并充分加热的原因是

[交流讨论]
甲同学:根据此实验测得的数据,计算硫酸铵化肥的氮含量可能偏高,因为实验装置中存在一个明显缺陷是 
乙同学:实验装置中还存在另一个明显缺陷是:

经过大家充分讨论一致认为:针对甲、乙两位同学指出的实验装置中存在的明显缺陷,需改进实验装置,重新进行实验。
[探究结论]
称取13.5g硫酸铵化肥样品,用改进后的实验装置重新进行实验,测得实验前后B装置增重3.40g。该化肥_________(填“是”或“不是”)一等品。


17.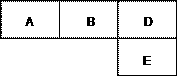 (8分)有M、A、B、D、E五种短周期元素,原子序数依次增大。
(8分)有M、A、B、D、E五种短周期元素,原子序数依次增大。
M元素的单质是自然界最轻的气体。A、B、D、E分别在右表(周期表
16.下列离子方程式,正确的是( )
A.Ca(ClO)2溶液中通入少量SO2气体
H2O +SO2
+ Ca2+ + 2ClO- === CaSO3↓+ 2HClO
B.向NH4HCO3 溶液中加入足量Ba(OH)2溶液
NH4+ +HCO3-
+ 2OH- === H2O + CO32- + NH3·H2O
C.向FeCl2溶液中加足量溴水
2Fe2+ + Br2
=== 2Fe3++ 2Br-
D.NaAlO2溶液中通入过量CO2
2AlO2-
+CO2+3H2O===2Al(OH)3↓+CO32-
15.背景材料:① 2004年,诺贝尔化学奖授予研究蛋白质的科学家② 2005年,广东大部分地区进行人工降雨③ 2006年,湖北某高速公路的液氯运输车翻倒,发生泄漏事故④
2007年,法国科学家以CO2为碳源,Na为还原剂,在470℃,80MPa条件下合成出金刚石。下列说法不正确的是( )
A.蛋白质是由氨基酸形成的不可降解的高分子化合物,其水溶液有丁达尔现象
B.AgI和于冰都可用于人工降雨
C.远离液氯泄漏地点,附近的人员应迅速逆风往高处安全区疏散
D.用CO2合成金刚石时,Na被氧化成Na2CO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com