
题目列表(包括答案和解析)
29.(20分)
(1) Ⅲ (2分)
(2) 饱和NaHCO3 溶液 (2分) , 浓硫酸(2分)
(3) E (2分) ,浑浊(或大量白色沉淀生成) (2分) ,排出装置中的空气,以免空气中O2、H2O与钠反应,干扰实验。(2分)
(4) 2Na+2CO2=Na2CO3+CO (3分)
(5) 4Na+3CO2=2Na2CO3+C (3分)
(6) 取装置D中的残留固体在空气中加热,如果固体颜色由白色变为淡黄色说明有Na2O。(2分)
29. (20分)某化学兴趣小组的同学根据Mg能在CO2中燃烧的原理推测Na也能在CO2中燃烧,为验证推测的正确性,该小组设计了下列实验方案(已知PdCl2溶液能与CO反应生成黑色沉淀)。

请回答下列问题:
(1)按实验室制取CO2的方法,为了使反应能随开随用,随关随停,图一的虚线框内应选用图二中的 装置(填序号)。
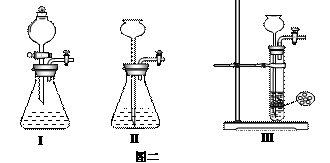
(2)装置B中应盛装 溶液,装置C中应盛装 溶液。
(3)实验时先检查装置气密性并装好药品,打开玻璃活塞,让生成的CO2充满整个装置,直到装置 (填字母编号)中出现 现象时,再点燃酒精灯。让CO2充满整个装置的目的是_______________________________________________________________。
(4)若装置F中有黑色沉淀生成,装置D的硬质玻璃管中残留的固体只含一种物质,该物质放入稀盐酸中有能使澄清石灰水变浑浊的气体生成,则装置D的硬质玻璃管中Na与CO2反应的化学方程式为 。
(5)若装置F中无明显现象,装置D的硬质玻璃管中残留的固体含有两种物质,把固体放入稀盐酸中也有能使澄清石灰水变浑浊的气体生成,则装置D的硬质玻璃管中Na与CO2反应的化学方程式为 。
(6)该小组的一位同学认为装置D的硬质玻璃管中残留物质还可能含有Na2O(假若Na已充分反应),请你帮助设计一个简单实验,验证装置D的硬质玻璃管中的残留固体是否含有Na2O:________________________________ ____________________
28.(10分)
(1) < (2分) (2) 不变 (2分) (3) > (2分)
(4) p=2 (2分) , x =1.6 (2分)
28. (10分)将m mol A 与n mol B 充入一密闭容器中,发生反应如下:
m A(g) + n B(g)  p C(g) ;△H = a kJ/mol ( a<0)
p C(g) ;△H = a kJ/mol ( a<0)
反应在一定条件下达到平衡,请回答下列问题:
(1) 若在恒温下增大压强,V正 < V逆 ,则m+n p(填“>” 、“<”或“=” )。
(2) 若保持恒温、恒压,向原平衡中再加入 p mol的C,重新达平衡后,C的体积分数将
(填“增大”、“减小”或“不变” )。
(3) 若在恒温、恒容下达到平衡时A的转化率为A1% ;在绝热、恒容条件下达到平衡时A的转化率为A2%,则A1 A2 (填“>” 、“<”或“=”)。
(4) 当m=2,n=1时,向原平衡中再加入 1 mol的B,重新达到平衡,A、B、C的物质的量之比为1∶3∶4,C的物质的量为 x mol,则p=_________ x=_________。
27.(14分)
 (1) Fe、CH CH (4分,每空2分)
(1) Fe、CH CH (4分,每空2分)
(2) 2Fe2++Cl2 = 2Fe3++2Cl- (2分)
(3) CaC2+2H2O C2H2↑+Ca(OH)2 (3分)
C2H2↑+Ca(OH)2 (3分)
(4) 5种 (2分)
(5) 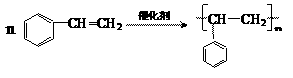 (3分)
(3分)
27. (14分)已知:X、Y、Z、W为有机物,其余为无机物,其中A、C、G为单质;Z的相对分子质量是X的4倍,且X、Z的最简式相同,W是苯的同系物。在一定条件下它们能实现如下图所示的转化关系(图中部分生成物已略去)。
试回答下列问题:
(1) A的化学式为_____ __,X的结构简式为_____ __ ___。
(2) 图中浅绿色溶液变为棕黄色溶液反应的离子方程式为 。
(3) 写出F与水反应生成X的化学方程式 。
(4) W的一氯取代物有 种。
(5) Z在离子型催化剂存在下可以聚合生成一种泡沫塑料,广泛应用于电视机、空调器的外壳,制作包装材料、容器和家具等。Z生成泡沫塑料的化学方程式为:
。
26.(16分)
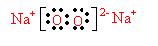 (1)第三周期,第ⅥA族 (2分)
(1)第三周期,第ⅥA族 (2分)
(2) 非极性 (2分), (2分),2Na2O2+2CO2 = 2Na2CO3+O2 (3分)
(3) 离子晶体 (2分) 碱性(2分)
(4) C2H6 + 18OH--14e- = 2CO32- + 12H2O (3分)
26.(16分)A、B、C、D是元素周期表中四种短周期元素,请根据表中信息回答下列问题:
|
元素 |
A |
B |
C |
D |
|
性质或结构信息 |
形成化合物种类最多的元素 |
最高正价是最低负价绝对值的3倍 |
族序数等于周期数的3倍 |
周期数是族序数的3倍 |
(1) 指出元素B在周期表中的位置 。(须指明周期和族)
(2) 元素A、D分别与元素C形成原子个数比为1∶2的化合物甲和1∶1的化合物乙,则甲属于_________分子(填“极性”或“非极性” ),乙的电子式为 ,甲与乙反应的化学方程式为 。
(3) 元素B、D组成化合物丙,其晶体类型为 ,化合物丙的溶液呈 (填“酸性”、“碱性”或“中性”)
(4) 元素A与氢元素组成化合物丁,其氢元素的质量分数为20%,由化合物丁、元素C的单质和元素D的最高价氧化物对应水化物的水溶液可构成原电池,则该电池的负极电极反应式为: 。
13. 在100 mL 18.5 mol/L的浓硫酸中加入一定量的锌,充分反应后,锌完全溶解,同时生成33.6L气体 (标准状况,假设SO2全部逸出)。将反应后的溶液稀释到1 L ,测得溶液的pH=1,则下列叙述错误的是
A.生成的气体是SO2和H2的混合物 B.反应的锌为97.5g
C.生成的气体中SO2和H2的体积比为1:3 D.反应中共转移电子3 mol
12. 某有机物结构简式为:有关它的说法正确的是
某有机物结构简式为:有关它的说法正确的是
A.它属于芳香烃 B.分子式为C16H14Br3
C.分子中最多有24个原子共面 D.1mol该物质能与6mol H2加成
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com