
题目列表(包括答案和解析)
4、蛋白质、糖类和脂肪通过消化液的消化作用,分解成溶于水的、能被吸收的小分子物质,这些小分子物质分别是: ( )
A、葡萄糖、麦芽糖、甘油和脂肪酸 B、氨基酸、葡萄糖、甘油和脂肪酸
C、氨基酸、葡萄糖和脂肪酸 D、氨基酸、麦芽糖、甘油和脂肪酸
3、2005年1月在广州发现了一种红色的蚂蚁,叫红火蚁,它们啃食植物的根甚至叮咬人体。医生告诫人们若被红火蚁叮咬,可在被叮咬过的皮肤处涂上肥皂水(显碱性)以消除痛痒,由此可知红火蚁叮咬时的分泌物PH为 ( )
A、<7 B、=7 C、>7 D、无法确定
2、NO对大气有污染,可它在生物学方面所起的独特功能,引起生物学界和医学界的极大关注,曾被誉为“明星分子”。NO属于 ( )
A、酸 B、碱 C、盐 D、氧化物
1、下列家用电器中,利用电流热效应工作的是 ( )
A. 电熨斗 B. 电风扇 C. 电冰箱 D. 电视机
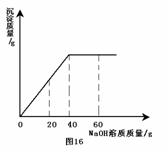
2. 某同学在实验室发现一瓶标签残缺(如图15所示)的溶液。为了测定此溶液的溶质质量分数,他取出50g该溶液,向其中逐滴加入溶质质量分数为10%的NaOH溶液。反应过程中生成沉淀的质量与所用NaOH溶液质量的关系如图16所示。请计算此硫酸镁溶液中溶质的质量分数。
某同学在实验室发现一瓶标签残缺(如图15所示)的溶液。为了测定此溶液的溶质质量分数,他取出50g该溶液,向其中逐滴加入溶质质量分数为10%的NaOH溶液。反应过程中生成沉淀的质量与所用NaOH溶液质量的关系如图16所示。请计算此硫酸镁溶液中溶质的质量分数。
1. 化学综合实践活动小组的同学,对一造纸厂排放的污水进行检测,发现其主要的污染物为氢氧化钠。为了测定污水中氢氧化钠的含量,他们用溶质质量分数为37%、密度1.18g/cm3的浓盐酸,配得溶质质量分数为5%稀盐酸200.0g。然后取80.0g污水于烧杯中,逐滴加入这种稀盐酸至73.0g时恰好完全反应(污水中的其它成分不与盐酸反应)。请计算:
(1)配制稀盐酸时,量取了溶质质量分数为37%的浓盐酸多少毫升?
(2)污水中所含氢氧化钠的质量分数是多少?
8. 镁将成为2 1世纪重要的轻型环保材料,我国含有非常丰富的镁资源。
(1)占地球表面积7 O%的海洋是天然的镁元素宝库,从海水中提取镁的流程如下:
熟石灰 盐酸 脱水



 海水中的MgCl2--------Mg(OH)2-------- MgCl2+6H2O
------MgCl2------Mg
海水中的MgCl2--------Mg(OH)2-------- MgCl2+6H2O
------MgCl2------Mg
①在实验室进行过滤操作时需要用到玻璃棒,其作用是__________________
②电解熔融氯化镁的过程中,_______能转化为__________能。
(2)①金属镁是一种较活泼金属,在二氧化碳气体中也能燃烧。燃烧的化学方程式为2 Mg+C02==C+2MgO,此反应类型属于 ( )A.分解反应 B.化合反应 C.置换反应 D.复分解反应
②金属镁在高温下与氮气反应生成氮化镁,在氮化镁中氮元素的化合价为一3。据此写出
氮化镁的化学式____________________________ 。
(3)镁铝合金广泛用于火箭、导弹和飞机制造业等。某兴趣小组为探究镁铝合金的组成,取
1 6 g镁铝合金样品,把6 0 g氢氧化钠溶液平均分成三份依次加入样品中(铝与氢氧化钠
溶反应的化学方程式为2 Al+2 NaOH+2H2O==2NaAl02+3H2↑,镁与氢氧化钠溶液不反应),充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
|
所加氢氧化钠溶液的次数 |
第一次 |
第二次 |
第三次 |
|
剩余固体的质量/g |
1 O.6 |
5.2 |
4.O |
从以上数据可知,该合金中,镁元素与铝元素的质量比为_____________
所用氢氧化钠溶液的溶质质量分数为_________________ 。
(4)老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属。但拿出的镁条总是有一层灰黑色的“外衣",这层灰黑色的外衣是什么物质呢?
猜想:小明认为可能是MgO;小赵认为可能是Mg2(OH)2 C03;小花认为可能是Mg(OH)2。
 小赵认为小明的猜想是错误的,其理由是_____________ 。
小赵认为小明的猜想是错误的,其理由是_____________ 。
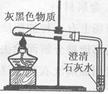
实验探究:小赵按右图所示装置进行实验,发现试管口有液滴出现,澄清石灰水变浑浊,同时试管内生成白色固体。实验分析:实验后,小赵认为小花的猜测也是错误的,其理由是_____________________,__________________________.查阅资料得出结论:
Mg(O H)2和Mg2(OH)2 C03都可以加热分解,产物均为氧化物,据此请你写出Mg2(OH)2 C03加热分解的化学方程式________.
7.(07威海)已知一种固体化合物由C、H、O、Cu四种元素组成。向盛有该化合物的试管中加入稀盐酸,产生大量气泡,固体逐渐溶解,得到蓝绿色溶液。己知这种蓝绿色是氯化铜溶液。
(1)探究产生的气体是什么。
[猜想]①可能是氢气;② ③ ……
[实验]请针对你②和③猜想中的一种,设计实验,验证你的猜想。 。
(2) 从蓝绿色溶液中提取金属铜。现利用该溶液制取金属铜,过程如下:

①操作1的名称为 ,完成该实验需要的主要仪器有 ,加入过量的A的目的是 ,反应化学方程式为 。
②加入足量B的目的是 ,如何确定此目的已经达到? 。
6.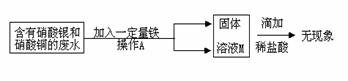 (07上海虹口)某工厂实验室的废水中含有大量的硝酸银和硝酸铜,某校兴趣小组对其进行了如下研究。
(07上海虹口)某工厂实验室的废水中含有大量的硝酸银和硝酸铜,某校兴趣小组对其进行了如下研究。
(1)操作A是_____________________
(2)溶液M中含有的溶质可能有哪些情况____ __
实验与探究
5.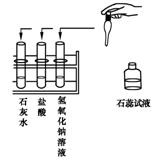 (07烟台)国家环保总局已规定将各类实验室纳入环保监管范围。某中学九年级甲、乙两个班的同学分别做常见酸和碱与指示剂反应的实验,所做
(07烟台)国家环保总局已规定将各类实验室纳入环保监管范围。某中学九年级甲、乙两个班的同学分别做常见酸和碱与指示剂反应的实验,所做
的实验和使用的试剂如图所示。实验后废液分别集中到各班的废液缸中,甲班废液呈红色,乙班废液呈蓝色。(1)请你分析废液的成分:甲班废液含有 ;乙班废液中含有 。
(2)目前许多高校、中学以及科研单位的化学实验室排放
的各类废液大都未经严格处理便进入了下水道。甲班的废液
若直接排入铸铁管下水道,会造成什么危害? ;
你建议如何处理甲班的废液? 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com