
题目列表(包括答案和解析)
13.已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下
(1)CuSO4+Na2CO3 主要:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑
次要:Cu2++ CO32-== CuSO3↓
(2)CuSO4+Na2S 主要:Cu2++S2-==CuS↓
次要:Cu2++S2-+2 H2O== Cu(OH)2↓+ H2S↑
下列几种物质的溶解度大小的比较中,正确的是 ( )
A.CuS<Cu(OH)2<CuCO3 B.CuS>Cu(OH)2>CuCO3
C.Cu(OH)2>CuCO3>CuS D.Cu(OH)2<CuCO3<CuS
12.下列各组离子,无论是在强酸性环境还是在强碱性环境均可大量共存的是 ( )
A.Na+、K+、HCO3-、NO3- B.Ba2+、Mg2+、SO42-、Cl-
C.Ag+、K+、Na+、NO3- D.K+、Na+、NO3-、Cl-
11. 在相同温度和压强下,对反应CO2(g)+H2 (g) CO(g)+H2O(g)进行甲、乙、丙、丁四
在相同温度和压强下,对反应CO2(g)+H2 (g) CO(g)+H2O(g)进行甲、乙、丙、丁四
组实验,实验起始时放入容器内各组分的物质的量见下表
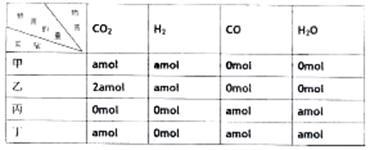
上述四种情况达到平衡后,n(CO)的大小顺序是 ( )
A.乙=丁>丙=甲 B.乙>丁>甲>丙
C.丁>乙>丙=甲 D.丁>丙>乙>甲
10. 将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2 (g)+Br2 (g) 2HBr(g)△H<0,
将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2 (g)+Br2 (g) 2HBr(g)△H<0,
g平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时 Br2(g)的
转化率为b,则a与b的关系是 ( )
A.a>b B.a=b C.a<b D.无法确定
9. 2NO2 2NO+O2在密闭容器中进行,达到平衡状态的标志是 ( )
2NO2 2NO+O2在密闭容器中进行,达到平衡状态的标志是 ( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示反应速率之比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
A.①④⑥ B.②③⑤ C.①③④ D.①②③④⑤⑥
11.2L气体(不考虑气体溶解)。下列叙述中不正确的是 ( )
A.阴极上有Cu析出
B.阴极上产生的气体是氢气
C.阳极上产生的气体是氯气和氧气混合气体
D.使溶液恢复到原来状态,需加入适量CuO并通适量HCl气体
8.用惰性电极电解250mLNaCl和CuSO4的混合溶液,经过一段时间后,两电极分别得到
7. 在密闭的容器中进行如下的反应H2(g)+I2(g) 2HI(g),在温度T1和T2时,产物的量和
在密闭的容器中进行如下的反应H2(g)+I2(g) 2HI(g),在温度T1和T2时,产物的量和
时间的关系如下图所示,符合图象的正确的判断是 ( )
 A.T1>T2,△H>0
A.T1>T2,△H>0
B.T1>T2,△H<0
C.T1<T2,△H>0
D.T1<T2,△H<0
6.X、Y、Z三种气体,取X和Y按1:1的物质的量之比混合,放入密闭容器中发生如下
 反应:X+2Y 2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总
反应:X+2Y 2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总
物质的量之比为3:2,则Y的转化率最接近于 ( )
A.33% B.40% C.50% D.65%
5.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4
氧化性更强,无二次污染的绿色处理剂。工业是先制得高铁酸钠,然后在低温下,在高
铁酸钠溶液中:
湿法制备的主要反应方程为: Fe(OH)3+ ClO-+ OH-=== FeO42-+ Cl-+ H2O
干法制备的主要反应为: FeSO4+ Na2O2=== Na2FeO4+ Na2O+ Na2SO4 + O2↑(均未配平)
下列有关说法不正确的是 ( )
A.高铁酸钾中铁显+6价
B.湿法中每生成1 mol Na2FeO4转移3 mol电子
C.干法中每生成1 mol Na2FeO4转移4 mol电子
D.K2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的
Fe(OH) 3还能吸附水中的悬浮杂质
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com