
题目列表(包括答案和解析)
8.已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。
下列反应在水溶液中不可能发生的是 ( )
A.3C12 + 6FeI2 = 2FeCl3 + 4FeI3 B.C12 + FeI2 = FeCl2 + I2
C.Co2O3+ 6HCl = 2CoCl2+Cl2 + 3H2O D.2Fe3+ +2I- = 2Fe2+ +I2
7.20℃时饱和KCl溶液的密度为1.174g/cm3,物质的量浓度为4.0 mol/L,则不正确的是( )
A.25˚C时,饱和KCl溶液的浓度大于4.0 mol/L
B.此溶液中KCl的质量分数为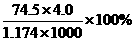
C.20℃时,密度小于1.174 g/cm3的KCl溶液是不饱和溶液
D.将此溶液蒸发部分水,再恢复到20˚C时,溶液密度一定大于1.174 g/cm3
6.若NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.7. 1g Cl2与足量NaOH溶液反应转移电子数为0.2NA
B.在25˚C,101kPa时,14g氮气中含有7NA个电子
C.在0˚C,101kPa时,含有NA个氢原子的氢气体积为22 .4L
D.标准状况下11.2LSO3所含的分子数为0 .5NA
5.下列说法正确的是 ( )
A.刚落下的酸雨酸性逐渐增强,是由于溶质被不断氧化的原因
B.从上到下,卤素的非金属性逐渐减弱,故氢卤酸的酸性依次减弱
C.因为氧化性:HClO>稀H2S04,所以非金属性:Cl>S
D.钠在反应中失去的电子比铝少,故钠的金属性小于铝的金属性
4.请你运用所学的化学知识判断,下列有关化学观念的叙述错误的是 ( )
A.几千万年前地球上一条恐龙体内的某个原子可能在你的身体里
B.用斧头将木块一劈为二,在这个过程中个别原子恰好分成更小微粒
C.一定条件下,金属钠可以成为绝缘体
D.一定条件下,水在20℃时能凝固成固体
3.下列说法正确的是 ( )
A.硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
B.蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
C.Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到
D.沼气、天然气和水煤气分别属于化石能源、可再生能源和二次能源
2.下列说法正确的是 ( )
A.硅是人类将太阳能转变为电能的常用材料 B.工艺师利用盐酸刻蚀石英制作艺术品
C.水晶项链和餐桌上的瓷盘都是硅酸盐制品 D.粗硅制备单晶硅不涉及氧化还原反应
1.图标 所警示的是 ( )
所警示的是 ( )
A.当心火灾一一氧化物 B.当心火灾一一易燃物质
C.当心爆炸--自燃物质 D.当心爆炸一一爆炸性物质
25.在50mLamol·L-1的硝酸溶液中,加入6.4gCu,全部溶解,假设硝酸的还原产物只有
NO2和NO,将反应后溶液用蒸馏水稀释至100mL时测得c(NO3-)=3mol·L-1
(1)求稀释后的溶液pH 。
(2)若a=9,则生成的气体中NO2的物质的量为 mol。
(3)治理氮氧化物污染的方法之一是用NaOH溶液进行吸收,反应原理如下:
NO2+NO+2NaOH====2NaNO2+H2O
2NO2+2NaOH====NaNO2+NaNO3+H2O
若将上述的NO2和NO的混合气体通入1 mol·L-1的NaOH恰好被吸收,求NaOH溶液
的体积 mL?
24.(12分)N2在化工生产、农业、医疗、航天航空等诸多领域用途广泛。某化学兴趣小组
同学为探究在实验室制备较为纯净N2的的方法,进行了认真的准备。请你参与交流与
讨论。
[查阅资料]N2的制法有下列三种方案:
方案1:加热条件下,以NH3还原CuO可制得N2,同时获得活性铜粉
方案2:加热NaNO2和NH4Cl的浓溶液制得N2。
方法3:将空气缓缓通过灼热的铜粉获得较纯的N2。
[实验准备]以实验室常见仪器(药品)等设计的部分装置如下图(有的夹持和加热仪器
未画出。)
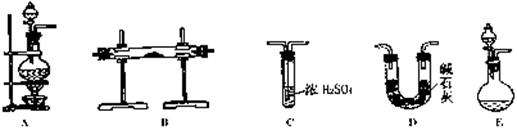
[分析交流]
(1)若按方案1制得干燥、纯净的N2,且需要的NH3以生石灰和浓氨水作原料,整套
制气装置按气流从左到右的顺序连接的顺序是(填写装置序号) ,获得
N2的反应原理是(写化学方程式) 。
(2)若以排水法收集N2,其中会混入水蒸气。但也不宜用排空气收集,其原因是 ,
你提出的收集方法是 。
(3)若以方案2制得N2,应选择的发生装置是(填装置序号) ,为使发生装置
能安全进行实验,可在烧瓶中先加入 。
(4)上述三个方案中,制得的N2纯度最低的是 。在N2纯度要求不甚严格的情
况下,有人建议将方案1和方案3结合使用,你认为其优点是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com