
题目列表(包括答案和解析)
15.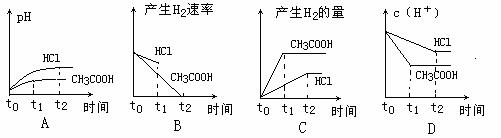 1L pH = 2的盐酸和醋酸溶液中,分别投入0.65g锌粒,则下图中比较符合客观事实的是:
1L pH = 2的盐酸和醋酸溶液中,分别投入0.65g锌粒,则下图中比较符合客观事实的是:
14.不久前,美国一个海军航空站安装了一台250kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600℃~700℃,所用燃料为H2,电解质为熔融的K2CO3,已知该电池的总反应为2H2 + O2====2H2O,负极反应为H2 + CO32--2e-====H2O + CO2,则下列推断正确的是
A.正极反应为:4OH-====O2+2H2O+4e-
B.放电时CO32-向负极移动
C.电池供应1 mol 水蒸气,转移的电子数4 mol
D.放电时CO32-向正极移动
13.A、B、C为第二、第三周期的元素,A、B在同周期,A、C最低价离子分别为A2-和C-,B2+和C-具有相同的电子层结构。下列说法中,正确的是
 A.原子核外最外层电子数:A>C>B B.离子半径:A2->C->B2+
A.原子核外最外层电子数:A>C>B B.离子半径:A2->C->B2+
C.B和C形成化合物的电子式为B2+[:C:]2 D.沸点:HC > H2A
12.有M、N两溶液,各含有下列十四种离子中的七种离子:Al3+、Cl-、Na+、K+、NO3-、OH-、S2-、MnO4-、Fe3+、NH4+、H+、SO42-、CO32-、AlO2-。已知两溶液所含离子各不相同,M溶液里的阳离子只有两种,则N溶液里的阴离子应该是
A.OH-、S2-、CO32- B. AlO2-、MnO4-、SO42-
C.Cl-、NO3-、SO42- D. MnO4-、SO42-、NO3-
11. 设NA为阿伏加德罗常数的值,下列叙述中正确的是
A.常温常压下,3.2g O3所含电子数为1.2NA
B.标准状况下,11.2L氯仿中含有的C-Cl键的数目为1.5NA
C.标准状况下,11.2L NO与11.2L O2 混合后所含原子数为2NA
D.电解精炼铜时,电解池中每转移1mol电子,阳极上溶解的铜原子数为0.5 NA
10.工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3,已知该反应为一放热反应。现将2mol SO2、1mol O2充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO2的转化率为50%,则下列热化学方程式正确的是:
A.2SO2(g) + O2(g) 2SO3(g) △H = -196.6kJ·mol-1
2SO3(g) △H = -196.6kJ·mol-1
B.2SO2(g)
+ O2(g) 2SO3(g) △H = -98.3kJ·mol-1
2SO3(g) △H = -98.3kJ·mol-1
C.SO2(g)
+ 1/2O2(g) SO3(g) △H = -98.3kJ·mol-1
SO3(g) △H = -98.3kJ·mol-1
D.SO2(g)
+ 1/2O2(g) SO3(g) △H = -196.6kJ·mol-1
SO3(g) △H = -196.6kJ·mol-1
9.相同温度下,将足量的AgCl分别放入下列溶液中:
① 20mL0.1mol/L(NH4)2CO3溶液 ②40mL0.02mol/LBaCl2溶液
③ 40mL0.03mol/L盐酸 ④10mL蒸馏水 ⑤50mL0.05mol/LAgNO3溶液
则AgCl的溶解度大小顺序为
A.① = ② = ③ = ④ = ⑤ B. ① > ④ > ③ > ② > ⑤
C.⑤ > ④ > ① > ③ >② D. ④ > ③ > ⑤ > ① > ②
8、 “喷水溶液法”是最近日本科学家研制出的一种使沙漠变绿洲的技术,它是先在沙漠中喷洒一定量的聚丙烯酸酯水溶液,水溶液中的高分子与沙土粒子结合,在地表下30-50cm处形成一个厚0.5cm的隔水层,既能阻止地下的盐分上升,又有拦截、蓄积雨水的作用,下列对聚丙烯酸酯不正确的说法是
A.单体的结构简式为CH2==CH-COOR
B.在一定条件下能发生加成反应
C.在一定条件下能发生水解反应
D.没有固定熔沸点
7.从矿物学资料查得,一定条件下自然界存在如下反应: 14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4 ,下列说法正确的是
A.Cu2S既是氧化产物又是还原产物 B. 5mol FeS2发生反应,有10mol电子转移
C. 产物中的SO42-离子有一部分是氧化产物 D. FeS2只作还原剂
6.广义的水解观认为,无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质。根据上述观点,下列说法不正确的是
A.CaO2的水解产物是Ca(OH)2和H2O2 B. NaClO的水解产物之一是HClO
C.PCl3的水解产物是PH3和HClO D.Mg3N2水解生成NH3和Mg(OH)2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com