
题目列表(包括答案和解析)
6. 可逆反应CO+NO2 CO2+NO的反应速率与反应物浓的关系为v=kc(NO2)。一定温度下,该反应在一定体积的密闭容器中达到平衡状态,此时向容器中充入一定量的CO气体,下列叙述错误的是 ( )
可逆反应CO+NO2 CO2+NO的反应速率与反应物浓的关系为v=kc(NO2)。一定温度下,该反应在一定体积的密闭容器中达到平衡状态,此时向容器中充入一定量的CO气体,下列叙述错误的是 ( )
A.正反应速率增大,平衡向正反应方向移动
B.浓度商Qc减小,平衡向正反应方向移动
C.反应物的焓增大,平衡向正反应方向移动
D.CO气体分压增大,平衡向正反应方向移动
5.用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池。以下有关该原电池的叙述正确的是 ( )
①在外电路中,电流由铜电极流向银电极
②正极反应为:Ag++e-=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
A. ①② B.②③ C.②④ D.③④
4.下列各组物质之间反应,调节反应用量,离子方程式不变的是 ( )
A.石灰水和SO2 B.Na[Al(OH)4]和CO2
C.Ba(OH)2溶液和H2SO4溶液 D.NaHCO3溶液和石灰水
3.设NA为阿伏加德罗常数,下列说法中正确的是 ( )
A.标准状况下,1L液态水中含有的H+数目大于10-7NA
B.足量Zn与一定量的浓硫酸反应,标准状况下产生22.4L气体时,转移的电子数为2NA
C.常温下,pH=1的醋酸溶液中,醋酸分子的数目一定大于0.1NA
D.1mol FeCl3水解生成NA胶体粒子
2.“三效催化转换器”可将汽车尾气中的有毒气体处理为无污染的气体,下图为该反应的微观示意图(未配平),其中不同符号的球代表不同种原子。下列说法不正确的是( )
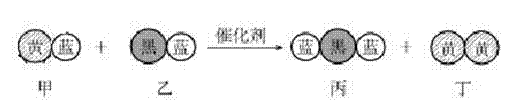
A.该反应属于氧化还原反应 B.甲和丙中同种元素化合价不可能相等
C.丁物质一定是非金属单质 D.配平后甲、乙、丙的化学计量数均为2
1.英国化学家波义耳1661年提出化学元素的概念,标志着近代化学的诞生。波义耳指出:我指的元素应当是某些不由任何其它物质所构成的原始和简单的物质或完全纯净的物质,是具有一定确定的、实在的、觉察到的实物,它们应该是用一般化学方法不能再分解为更简单的某些实物。从现代化学的观点看,波义耳定义的元素实际为 ( )
A.原子和分子 B.纯净物 C.单质 D.化合物
2.考生请将第I卷选择题的正确选项用2B铅笔涂写在答题卡上。考试结束后,只收答题卡和第II卷。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Na 23 Mg 24
Al 27 K 39 Fe 56 Cu 64
第I卷(选择题,共45分)
第I卷包括15小题,每小题3分,共45分。每小题只有一个选项符合题意。
1.本试卷包括第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分。考试时间90分钟。
28.现取等物质的量混合的氧气、氮气和二氧化碳气体a mol,压强为pPa,在固定容积的密闭容器中进行实验。
(1)若加入过量硫,加热条件下充分反应后,恢复到原温度,则压强是原来的 倍。
(2)若加入一定量的磷,加热条件下,充分反应生成P2O5后,恢复到原温度,压强是原来的3/4,则加入磷的质量为 。
(3)若加入b mol碳,高温条件下充分反应后,恢复到原温度,试计算反应后气体压强是原来的倍数。(写出计算过程)
27.(12分)已知A-L所代表的物质(或溶液中的溶质)都是中学化学课本里学过的物质。通常状况下,A、B是淡黄色固体,B是金黄色固体,俗称“愚人金”,D是单质气体,E是无色无味气体,K是不溶于水的酸。反应①一③是化学工业生产某重要产品的三步反应,反应④是工业生产普通玻璃的反应之一。一定条件下,各物质间的相互转化关系如图所示(反应时加入或生成的水均没标出)
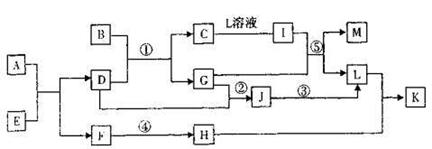
请回答:
(1)写出下列物质的化学式:B ;D的同素异形体
(2)写出A的电子式 ;E的电子式
(3)指出反应①、②、③是吸热反应,还是放热反应
① ② ③
(4)完成下列反应方程式:
反应⑤的离子方程式:
反应④的化学议程式为 。
(5)15.6克A与适量E完全反应,转移的电子的物质的量为
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com