
题目列表(包括答案和解析)
6.下列有关试剂的保存方法中,错误的是
A.NaOH溶液存放在带橡胶塞的细口瓶中 B.金属钠浸在盛有四氯化碳的广口瓶中
C.浓硝酸存放在棕色试剂瓶中 D.溴水存放在带玻璃塞的细口瓶中
5.下列说法中正确的是
A.非自发反应在任何条件下都不能实现
B.自发反应一定是熵增大,非自发反应一定是熵减小或不变
C.凡是放热反应都是自发的,吸热反应都是非自发的
D.熵增加且放热的反应一定是自发反应
4.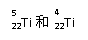 金属钛对体液无毒且惰性,能与肌肉和骨骼生长在一起,有“生物金属”之称。下列有关
金属钛对体液无毒且惰性,能与肌肉和骨骼生长在一起,有“生物金属”之称。下列有关
 的说法中,正确的是
的说法中,正确的是
 A.原子中均含有22个中子
B. 在周期表中位置相同
A.原子中均含有22个中子
B. 在周期表中位置相同
 C.分别由
组成的金属钛单质化学性质不相同
C.分别由
组成的金属钛单质化学性质不相同
D. 为同一核素
3.用右图表示的一些物质或概念间的从属关系中,不正确的是
|
|
X |
Y |
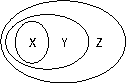 Z Z |
|
A |
甘油 |
化合物 |
纯净物 |
|
B |
胶 体 |
分散系 |
混合物 |
|
C |
电解质 |
离子化合物 |
化合物 |
|
D |
碱性氧化物 |
金属氧化物 |
氧化物 |
2.下列各组混合物可用加热方法分离的一组是
①NH4HCO3和NaHCO3 ②NaCl和I2 ③NH4Cl和NaCl ④KClO3和KCl
A.②③ B.②④ C.②③④ D.①②③④
1.下列有关生活中的化学常识说法,错误的是
A.为保证加酶洗衣粉的洗涤效果,应使用沸水冲泡洗衣粉
B.用多聚氯化铝净化水
C.用食醋可除去水壶中的水垢
D.长期用铁强化酱油作佐料,可预防缺铁性贫血
20.(8分)如图:横轴表示溶液的pH,纵轴表示Zn2+离子或[Zn(OH)4]2-离子(配离子)
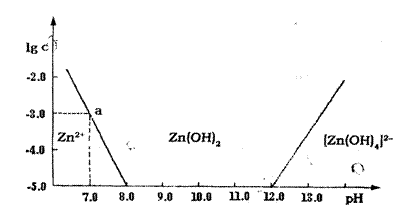 物质的量浓度的对数,回答下列问题。
物质的量浓度的对数,回答下列问题。
(1)往ZnCl2溶液中加入过量的氢氧化钠溶液,反应的离子方程式可表示
。
(2)从图中数据计算可得Zn(OH)2溶度积(Ksp)= 。
(3)某废液中含Zn2+离子,为提取Zn2+离子可以控制溶液的pH的范围是 。
(4)往1L1.00mol·L-1ZnCl2溶液中加入NaOH固体至pH=6,需NaOH= mol(精确到小数点后2位,忽略溶液体积变化)。
19.(14分)某学习小组在实验室条件下,用标准卷尺、中学化学实验室常用的托盘天平和如图所示的仪器,以及稀硫酸和宽度、厚度均匀的纯镁带测定气体摩尔体积,假如实验是在标准条件下进行,试回答下列问题:
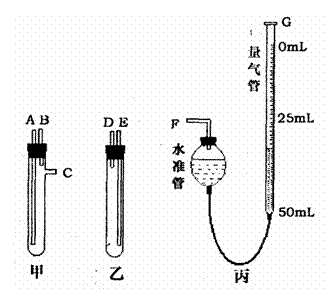
(1)甲乙两试管各有两根导管,用橡胶管连接对应接口后,若倒置盛稀硫酸的试管,可发生反应放出气体。镁带和稀硫酸应分别置于 、 仪器中(填仪器编号);接口的连接方式是:A接 ,B接 ,C接 (填写各接口的编号)
(2)仪器丙由左右两部分组成,它们用橡胶管连通,并装入适量水(含少量食盐)。G管可以用化学实验室中的一种常用仪器改装,该仪器的名称是 。反应结束后读数时,除应将温度恢复至0℃,还应采取的措施是 。
(3)实验中到取用一定质量的镁带入试管中,取用的质量应小于 g;取用实验需要的镁带,能否用化学实验室常用的托盘天平 ,理由是 ;正确取用镁带的方法是 。
(4)如果镁带长Lm,质量为mg。实验中截面镁带长xcm,产生气体的体积为VmL,则测得标况下气体摩尔体积应表示为V(m)= 。
(5)实验中若取用的镁带表面部分被氧化,则导致测定结果 ;若稀硫酸取用不足量,则导致测定结果 ;若读数时量气管内液面变于水准管内液面,则导致测定结果 (填偏高、偏低或无影响)。
18.(13分)工业生产硝酸铵的流程图如下:
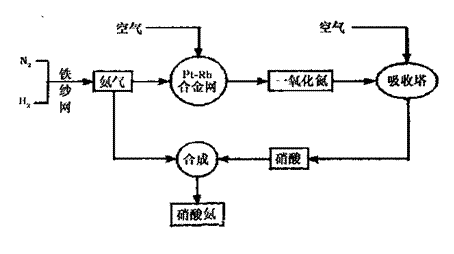
请回答下列问题:
 (1)已知N2(g)+3H2(g) 2NH3(g),△H=-92.4kJ·mol-。请回答:
(1)已知N2(g)+3H2(g) 2NH3(g),△H=-92.4kJ·mol-。请回答:
①在500℃、200atm和铁催化条件下向一密闭容器充入1molN2和3molH2,充分反应后,放出的热量 92.4kJ(填“<”“>”“=”),理由是
。
②为有效提高合成氨反应的速率,实际生产中宜采取的措施有 。
A.降低温度 B.最适合催化剂活性的适当高温
C.增大压强 D.降低压强
E.循环利用 F.原料氢中氮气和氢气的配比为1:2.8
G.及时分离出氨
(2)已知氨的催化氧化反应发生后,不需要继续加热,铂铑合金网仍然会保持红热。试写出该反应的化学平衡常数表达式K= ,当温度升高时,K值 (增大、减小、无影响),其原因是 。
(3)常温下某无色透明溶液中仅含有NH+4和NO-3等四种离子,请回答下列问题:
①该溶液所含的离子中除上述两种外还应有 (填离子符号)两种离子。
②该溶液所含的上述四种离子的物质的量浓度大小有多种可能。例如,可以是
c(NO-3)>c(NH+4)>c(H+)>c(OH-),也可以是c(NO-3)>c(H+)>c(NH+4)>c(OH-)
请你再填写两种可能 , 。
③如溶液中c(NH+3)=c(NO-3),则溶液中的溶质为 (填化学式),该溶液的pH= (填<、>或=)
17.(12分)黑火花是我国古代科技四大发明之一,在化学史上占有重要地位。黑火花主要是硝酸钾、硫磺、木炭三者粉末的混合物,在点燃条件下,其化学反应式主要为:
KNO3+S+C→N2↑+CO2↑+K2S
试填写下列空白:
(1)在黑火药燃烧的反应中,氧化剂为 ,被氧化的物质为 。
(2)黑火花的传统配方为“一硝二磺三木炭”,指的是KNO3、S和C的质量比。根据化学反应式分析,KNO3、S和C恰好完全反应时,它们的物质的量之比为 。
(3)对黑火药燃烧的反应,下列叙述错误的是 (填字母)
A.黑火花的焓比生成物的焓大
B.黑火花燃烧后,物质的化学能降低,化学能转变为热能、光能
C.该反应为自发反应,因为反应的△H<0,△S>0
D.该反应不是自发反应,因为反应必须在点燃条件下发生
(4)黑火花燃烧后的固体残留物中,除了K2S外,还有少许K2CO3、K2SO4和未燃烧的炭末。请设计一个简单的实验证明,黑火花燃烧的固体产物中存在K2S、K2CO3和K2SO4。
[实验方案]
(i) ;
(ii)用洁净的铂丝蘸取滤液,将铂丝放在酒精灯上焰上灼烧,透过蓝色钴玻璃片观察火焰,若火焰呈紫色,则证明含K+;
(iii) ,得到白色沉淀;
(iv) ;
(v) 。
(5)硝酸钾与木炭混合点燃,即可见到焰火。试综合上述有关信息,推断硝酸钾与木炭
的化学反应式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com