
题目列表(包括答案和解析)
11.在常温下,在由水电离出来的c(H+) = 10-2.5mol/L的溶液中,下列各组离子可能大量共存的是( )
A.Ag+、K+、Ba2+、I- B.AlO2-、S2-、PO43-、Na+
C.NH4+、Fe3+、Br-、SO42- D.Fe2+、Cu2+、Mg2+、NO3-
10.已知酸式盐NaHB在水溶液中存在下列反应:①NaHB==Na++HB-,
②HB-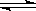 H++B2-,③HB-+H2O
H++B2-,③HB-+H2O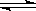 H2B+OH-且溶液中c(H+)>c(OH-),则下列说法一定正确的是( )
H2B+OH-且溶液中c(H+)>c(OH-),则下列说法一定正确的是( )
A.NaHB为强电解质 B.H2B为强酸
C.H2B为弱电解质 D.HB-的电离程度小于HB-的水解程度
9.在给定条件下,下列加点的物质在化学反应中能被完全消耗的是 ( )
A.用50mL8 mol·L-1 浓盐酸与10g二氧化锰共热制取氯气
B.标准状况下,将1g铝片投入20mLl8mol·L-1的硫酸中
C.向100mL3 mol.L-1的硝酸中加入5.6g铁
D.在5×107Pa、500 ℃和铁触媒催化的条件下,用氮气和氢气合成氨
8.两瓶气体分别为NO2和Br2蒸气,外观均相同,某同学设计了各种鉴别法,①用湿润的淀粉KI试纸②加少量NaCl溶液③加少量AgNO3溶液④加少量水后再加适量苯⑤一定条件下改变温度 ( )
A.只能采用①③④ B.只能采用②③④
C.能采用②③④⑤ D.都可以
7.下列数据是对应物质的熔点
|
Na2O |
NaCl |
AlF3 |
AlCl3
|
|
920 |
801 |
1291 |
190 |
|
BCl3 |
Al2O3
|
CO2 |
SiO2 |
|
-107 |
2073 |
-57 |
1723 |
据此做出的下列判断中错误的是 ( )
A.铝的化合物的晶体中有的是离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
6.常温下单质硫主要以S8形式存在。加热时,S8会转化为S6、S4、S2等。当温度达到750℃时,硫蒸气主要以S2形式存在(占92%)。下列说法中正确的是( )
A.S8转化为S6、S4、S2属于物理变化
B.不论哪种硫分子,完全燃烧时都生成SO2
C.常温条件下单质硫为原子晶体
D.把硫单质在空气中加热到750℃即得S2
5.下列实验操作会引起测定结果偏高的是( )
A.测定硫酸铜晶体结晶水含量的实验中,晶体加热完全失去结晶水后,将盛试样的坩埚放在实验桌上冷却
B.中和滴定用的锥形瓶加入待测液后,再加少量蒸馏水稀释
C.为了测定一包白色粉末的质量,将药品放在右盘,砝码放在左盘,并需移动游码使之平衡
D.配制物质的量浓度的溶液,定容时仰视刻度线
4.下列叙述正确的是 ( )
A.有单质参加或单质生成的化学反应一定是氧化还原反应
B.生成物只有一种的化学反应不一定是化合反应
C.生成阳离子的反应一定是氧化反应
D.有电解质参加的化学反应一定可以用离子方程式表示
3.在化学学科中经常使用下列物理量,其中跟阿佛加德罗常数(NA)无关的组合是:
①相对原子质量(Mr) ②摩尔质量(M) ③原子半径(r) ④键能(E) ⑤物质的量(n) ⑥化学反应速率(v) ⑦气体摩尔体积(Vm) ⑧溶解度(S) ⑨燃烧热(△H) ⑩溶质的质量分数(w)( )
A.①③⑧⑩ B.②④⑤⑥⑦⑨
C.①②③④⑤ D.⑥⑦⑧⑨⑩
2.“纳米材料”(1nm=10-9m)是当今材料科学研究的前沿,其研究成果广泛应用于催化及军事科学中。“纳米材料”是指研究开发直径为几纳米至几十纳米的材料,如将“纳米材料”分散到液体分散剂中,对于所得分散系的叙述正确的是 ( )
①所得物质一定是溶液 ②能全部透过半透膜 ③有丁达尔现象 ④所得液体可以全部透过滤纸
A.①② B.②③ C.①④ D.③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com