
题目列表(包括答案和解析)
29.氮化硅是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
□ +□C+□N2 □Si3N4+□CO
□Si3N4+□CO
(1)补充并配平上述反应的化学方程式(填写化学式和化学计量数)。
(2)该反应的平衡常数表达式为K =_______________________;升高温度时平衡常数减小,则其反应热DH________零(填“大于”、“小于”或“等于”);若在一定温度下,当上述反应达到平衡时增加氮气的流量,平衡常数将 (填“增大”、“减小”或“不变”)。
(3)当制得14 g Si3N4时,碳作为 剂将 (填“得到”或“失去”)
mol电子,所得的CO为 产物(填氧化或还原); 增加碳的用量时平衡
(填“正向移动”、“逆向移动”或“不移动”)。
28.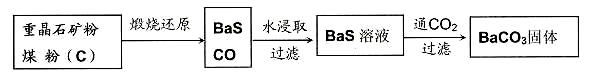 重晶石(BaSO4)难溶于水,要转化成BaCO3再制备其他钡盐。工业上一般采用高温煅烧还原法,其原理如下图所示。
重晶石(BaSO4)难溶于水,要转化成BaCO3再制备其他钡盐。工业上一般采用高温煅烧还原法,其原理如下图所示。
(1)煅烧还原的热化学方程式为:
有关的数据:Ba(s)+S(s)+2O2(g)=BaSO4(s);△H= -1473.2 kJ·mol-1
C(s)+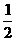 O2(g)=CO(g);△H= -110.5
kJ·mol-1
O2(g)=CO(g);△H= -110.5
kJ·mol-1
Ba(s)+S(s)=BaS(s);△H= -460kJ·mol-1
(2)经检验BaS的水溶液呈碱性,原因是(用离子方程式表示)
27.有1、2、3、4号4瓶未知溶液,它们是NaCl(0.1mol/L)、HCl(0.1mol/L)、NaOH(0.1mol/L)和酚酞(0.1%)。有人不用其他试剂,就把它们一一鉴别开来了,其实验步骤如下:
⑴各取溶液少许两两混合,据此分成两组。
⑵取一组混合液,不断滴入另一组的一种未知溶液,据此可鉴别出1号和2号。
⑶再取已鉴别出的1号2mL,滴入3滴3号未知液,再加入4号未知溶液4mL,在这个过程中无明显实验现象。
综合以上实验,可以确定1号是 ,2号是 ,3号是 ,4号是 。
26.依据氧化还原反应:2Ag+(aq)+Cu(s) = Cu2+(aq)+2Ag(s)设计的原电池如图所示。


请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是___________;
(2)银电极为电池的________极,发生的电极反应为______________________________;
X电极上发生的电极反应为____________________________;
(3)当Ag+的消耗速率为0.05mol/(L·min)时,Cu2+的生成速率是 。
(4)铜与盐酸的反应可用于设计原电池吗?简述原因。
25.填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的化学符号: 。
(2)周期表中位于第8纵行的铁元素属于第 族。
(3)周期表中最活泼的非金属元素位于第 纵行。
(4)所含元素超过18种的周期是第 、 周期。
24.下列叙述中不正确的是
A.在0.1 mol/L CH3COOH溶液中,c(H+)=c(CH3COO-)+c(OH-)
B.常温下将10 mL 0.02 mol/L NaOH溶液与10 mL 0.02 mol/L H2SO4溶液充分混合,
若混合后溶液的体积为20 mL,则混合后溶液的pH=2
C.在0.1 mol/L NH4Cl溶液中,c(H+)=c(NH3·H2O)+c(OH-)
D.在0.1 mol/L Na2CO3溶液中,2c(Na+)=c(H2CO3)+c(CO32-)+c(HCO3-)
第Ⅱ卷(非选择题,共52分)
23.将pH=3的盐酸aL分别与下列三种溶液混合后,溶液均呈中性:
①1×10-3mol·L-1的氨水bL ②c(OH-)=1×10-3mol·L-1的氨水cL
③c(OH-)=1×10-3mol·L-1的Ba(OH)2溶液d L
其中a、b、c、d的关系正确的是
A.b>a>d>c B.b>a=d>c
C.a=b>c>d D.c>a=b>d
22.下列图像正确反映所对应实验的是
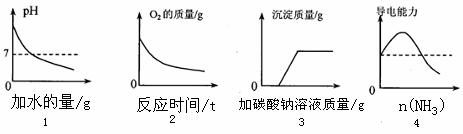
A.①为向pH=13的NaOH溶液中不断加水
B.②为向MnO2中加入一定量的H2O2溶液
C.③为向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液
D.④为将氨气通入醋酸溶液中
21.为确定某溶液的离子组成,进行如下实验: ①测定溶液的pH,溶液显强碱性。 ②取少量溶液加入稀盐酸至酸性,产生无刺激性、能使澄清石灰水变浑浊的气体。 ③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀。 ④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再加Ag NO3溶液,产生白色沉淀。 根据实验以下推测正确的是 A.一定有SO32-离子 B.一定有CO32-离子 C.Cl-离子一定存在 D.不能确定HCO3-离子是否存在
20.在一密闭容器中加入一定量的X,发生可逆反应:
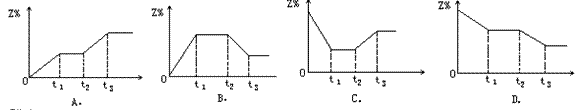 2X(气)
2X(气) 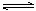 2Y(气)+Z(气) △H=Q kJ·mol-1(Q<0)在t1时刻达到平衡,然后在t2时刻开始加热到一定温度后停止加热并保温,到t3时刻又建立平衡,下图能表示这一变化的是
2Y(气)+Z(气) △H=Q kJ·mol-1(Q<0)在t1时刻达到平衡,然后在t2时刻开始加热到一定温度后停止加热并保温,到t3时刻又建立平衡,下图能表示这一变化的是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com