
题目列表(包括答案和解析)
|
|
|
|

|
|


|
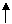
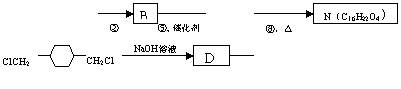
请回答下列问题:
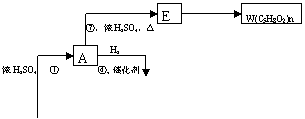
⑴W的结构简式为 。
⑵反应①-⑦中属于取代反应的有 。
⑶写出下列反应的化学方程式:
反应③:
反应⑥:
⑷M存在多种同分异构体,其中能发生银镜反应、含有1个“-OH”和2个“-CH3”的
酯的结构简式为 。
26.(12分)在室温下:3Cl2+2NH3 -- N2+6HCl
|
 NH3·H2O
NH3+H2O
NH3·H2O
NH3+H2O
根据上述原理,制取纯净干燥的N2;现有附图所示的仪器:
并有以下药品:①饱和食盐水;②浓硫酸;③浓硝酸;④稀盐酸;⑤稀NaOH溶液;⑥固体NaOH;⑦固体MnO2;⑧无水氯化钙;⑨浓氨水;⑩固体NaCl
设计制取过程是:
 制纯净干燥的Cl2气
制纯净干燥的Cl2气

 制N2 制纯净干燥的N2
制N2 制纯净干燥的N2
制纯净干燥的NH3气
请回答下列问题:
⑴从上述所列仪器中选出合适的几种,按顺序分别组成制氯气和制氨气(均要求干燥纯净)的两组连续装置,及各仪器中应选用的药品,将编号填入下表
|
制 Cl2 |
仪器编号 |
|
|
|
|
|
对应放入药品编号 |
|
|
|
|
|
制 NH3 |
仪器编号 |
|
|
|
|
|
对应放入药品编号 |
|
|
|
|
(以上两表不需填满,有几组填几组)
⑵制取氯气的反应原理是(用化学方程式表示):
⑶制取氨气时,固体NaOH的作用是:
⑷将干燥纯净的Cl2和NH3两种气体同时通入仪器 中(选填仪器编号)进行反应。
a.反应混合气体的成分:当进入反应装置的Cl2和NH3的物质的量之比小于
时,反应混合气体中一定含有NH3气,当它们的物质的量之比大于 时,反应混合气体中一定含有Cl2气。
b.实际上,制得的氮气中会含有少量NH3或Cl2气体,为了得到干燥纯净的N2气,可将混合气体先通过 ,再通过 (选填药品编号)。
25. 下列实验操作中,所用仪器不合理的是
A.用25mL的碱式滴定管量取14.80 mL NaOH溶液
B.用100 mL量筒量取5.2 mL盐酸
C.用坩埚加热K NO3溶液制取K NO3晶体
D.用100 mL容量瓶配制某实验需要使用的50 mL 0.10 mol·L-1的盐酸
E.用带橡皮塞的棕色试剂瓶存放浓硝酸
F.用50 mL蒸馏烧瓶加热40 mL乙酸乙酯和醋酸的混合液分离乙酸乙酯
24.将 a mol H2S和 1 mol O2置于一个容积可变的密闭容器中,维持容器压强为101 KPa不变,在120℃下测得反应容器内气体的密度分别为d1和d2,随a的取值不同,则H2S的氧化产物可能有如下三种情况:
⑴全部是SO2,此时a的取值范围是 ;
⑵全部是时S时,d1 d2 (填>,=,或<)
⑶既有SO2,也有S,a的取值范围是 ,容器内气体的平均摩尔质量为
(以含a的代数式表示)
23.化合物CO、HCOOH和HOOC-CHO(乙醛酸)分别燃烧时,消耗O2和生成的CO2的体积比(相同条件下),都是1∶2,后两者的分子式可以分别看成(CO)(H2O)和(CO)2(H2O)。
也就是说:只要分子式符合[(CO)n(H2O)m](n,m为正整数)的各种有机物,它们燃烧时消耗O2和生成的CO2体积比总是1∶2
现有一些只含C、H、O三种元素的有机物,它们燃烧时消耗O2和生成的CO2体积比是3∶4
⑴这些有机物中,相对分子质量最小的化合物的分子式是
⑵有两种碳原子数相等的上述有机物,若它们的相对分子质量分别为a和b(a<b),则
b-a必定是 (填一个数字)的整数倍。
22.关于相同温度下物质的量浓度相同的NaCl溶液和 NaClO溶液的叙述正确的是:
A.NaCl溶液中的c(Cl-)等于NaClO溶液中的c(ClO-)与c(HClO)之和
B. NaCl溶液中离子的总浓度小于NaClO溶液中离子的总浓度
C.两溶液中的c(H+)与c(OH-)之和相等
D. NaCl溶液的PH大于NaClO溶液的PH
高2009届高三上学期期中考试化学试题
班级 学号 姓名 得分
Ⅱ卷
21. 将50%的硫酸溶液和10%的硫酸溶液等体积混合,已知混合前后溶液的密度均大于1g/cm3,则混合溶液中溶质的质量分数为:
A. 大于30% B. 小于30% C. 等于30% D. 无法判断
20. 自然界中存在一种尖晶石,主要成分的化学式可表示为MgAl2O4,可作为宝石。已知该尖晶石中混有Fe2O3。取一定量样品54g,恰好完全溶解在一定浓度100mL盐酸溶液中,则盐酸的浓度可能是:
A. 2.2 mol/L B. 2.8 mol/L C. 4.3 mol/L D. 4.9mol/L
19.广义的水解观认为,无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质。根据上述观点,下列说法中,不正确的是:
A.CaO2的水解产物是Ca(OH) 2和H2O2
B. NaClO的水解产物之一是HClO
C. PCl3的水解产物是PH3和HClO
D. Mg3N2 水解生成NH3和Mg(OH) 2
18.X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是:
A.由mXa+与nYb-,得m+a = n-b
B.X2-的还原性一定大于Y-
C.X、Y一定不是同周期元素
D.若X的原子半径大于Y,则气态氢化物的稳定性HmX一定大于HnY
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com