
题目列表(包括答案和解析)
3.下列是同系物的是( )
A.CH4、C10H22 B.CH4、C2H5OH C.C3H6、C4H10 D.CH3COOH、C3H8
2.等物质的量的下列各烃,完全燃烧,生成CO2和H2O,耗氧量最多的是( )
A.CH4 B.C2H4 C.C6H6 D. C4H10
1.下列物质的说法不正确的是( )
A.天然气的主要成份是乙烯
B.芳香烃主要来自于煤的干馏后的煤焦油
C.汽油、煤油、柴油主要来自于石油的常压蒸馏
D.乙烯是石油裂解后的产物
25.
(1)空间利用率最低的是 (填字母),由非密置层互相错位堆积而成的是 。
(2)金属钛的晶胞为B型,其堆积方式的名称为 。
(3)R金属的密度 。(要求:①用含r、M、NA字母的式子表示②写出计算过程)
24.(11分)
(1) N2O的电子式可表示为 ,由此可知它 (填“含有”或“不含”)非极性键。
(2)①HFO的电子式为 , HFO的结构式,并标出HFO中各元素的化合价 。
②次氟酸的名称是否妥当?为什么? 。
③次氟酸与水反应的化学方程式为 。
23.(8分)
(1)水合氢离子(H3O+),其中含有的化学键有 、 。
(2)与冰的晶体类型相同的是______ (请用相应的编号填写)
(3)冰晶体中氢键的“键能”是 kJ/mol;
22.(6分)
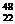 Ti和
Ti和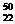 Ti两种原子,它们互称为
。元素周期表中的位置是第
周期,
Ti两种原子,它们互称为
。元素周期表中的位置是第
周期,
第 族;基态原子的电子排布式为 ;属于 区元素。
21.(14分)
(1)A是________,B是________,C是________,D是________,E是_________。
(2)简单离子按半径由小到大的顺序为(用离子符号表示)__________________________。
(3)B与D的电负性的大小关系是___________,C与E的第一电离能的大小是___________。(填﹥、﹤、﹦,用元素符号表示)
(4)用轨道表示式表示D元素原子的价电子构型____________________。
(5)写出A和B按原子个数比1 : 1形成的化合物的电子式 。
(6)用电子式表示D和E形成离子化合物的形成过程 。
20.(12分)
(1)元素是(填元素符号) ;
元素j的最高氧化物的化学式为 ,元素i最高氧化物的水化物的化学式为 。
(2)R的原子序数为(用p的代数式表示) ,R氢化物的化学式为 。
(3)m原子的外围电子排布式 。
25.下图所示为金属原子的四种基本堆积模型,请回答以下问题:
A.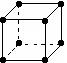 B.
B.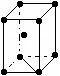 C.
C.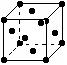 D.
D.
(1)以上原子堆积方式中,空间利用率最低的是 (在上图中选择,填字母),由非密置层互相错位堆积而成的是 。
(2)金属钛的晶胞为B型,其堆积方式的名称为 。
(3)某金属R的晶胞为D型,已知R原子半径为r cm,相对原子质量为M,阿佛加得德罗常数为NA,则R金属的密度 。(用含r、M、NA字母的式子表示)
注:本试卷分Ⅰ和Ⅱ两部分,请将Ⅰ卷答案填涂在答题卡上,Ⅱ卷填写在答卷纸上。
Ⅱ卷(共63分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com