
题目列表(包括答案和解析)
6.(11分)(1)将盛满氯水的无色矿泉水瓶倒置在水槽中,光照一段时间后,瓶底有无色气体生成。将瓶子倒转过来,用带火星的木条在瓶口检验气体,若木条复燃,证明HClO分解生成的气体为氧气。(3分)(2)提出假设:①氯气使布条褪色 ② HClO使布条褪色 ③盐酸使布条褪色(3分)
验证假设:②把红色布条伸入稀盐酸中,红色布条不褪色(1分)
结论:次氯酸使布条褪色(1分)
(3)①Cl2+2CO32-+H2O=2HCO3-+Cl-+ClO- (各1分)
②Cl2+CO32-+H2O=HCO3-+Cl-+HclO ③2Cl2+CO32-+H2O=CO2↑+2Cl-+2HClO
5.(12分) (1)c (1分)
(2)①(Ⅰ)饱和碳酸氢钠溶液; (Ⅱ)吸收未反应的NH3(答“防止倒吸”或“吸收CO2”不给分));
(Ⅲ)过滤 (每空1分,共3分)
②(Ⅰ)a、NH3, b、CO2; (每空1分,共4分)
(Ⅱ)增大气体与溶液接触面积,提高CO2吸收率; (2分)
(3)用碳酸氢铵与适量饱和食盐水反应。(或往烧碱溶液中通入过量CO2 ;往饱和Na2CO3 溶液中通入过量CO2 等。其他合理方法均可) (2分)
4..(10分)
(1)增大反应物接触面积,提高反应速率,提高原料的利用率(2分)

3.(1)溶液显色所需要的时间
(2)①2CO+2NO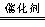 N2+2CO2 NO
②-1160 kJ·mol-1
N2+2CO2 NO
②-1160 kJ·mol-1
(3)①该研究只能提高化学反应速率,不能使化学平衡发生移动 ②6g
(每空2分,共12分)
2.(14分)
(1)冷凝、回流(1+1分)。防止倒吸(2分)。
|
(2)S+2H2SO4(浓) 3SO2↑+2H2O(2分,无加热符号、气体符号扣1分)
(3)取样后,向其中加入氯氧化钠溶液,观察是否有沉淀生成。(或者加热、加盐酸检验SO2气体等方法,开放题,正确即可)(2分)
(4)CuO、CuS、Cu2S(或CuO、CuS可CuO、Cu2S)(2分)
(5)铜与浓硫酸反应的实验中硫酸过量使溶液呈酸性(2分)。取稀释后的溶液适量于试管中,加入足量的铁粉,若有无色无味的气体产生,证明硫酸过量(开放题,正确即可)
1.(10分)(1)漏斗、烧杯、玻璃棒
;(2)2Fe(OH)3 Fe2O3+3H2O
Fe2O3+3H2O
(3)将所得的滤液E加热煮沸一定时间(或向滤液中加入足量的NaOH溶液),
再进行过滤、洗涤、干燥,最后进行高温灼烧。
(4)根据表中数据,控制溶液的pH在7~8之间,Mg2+没有变化,Al3+转化为AlO2- ,
只有Fe(OH)3沉淀。(5)8MgO·Al2O3·Fe2O3·4Si
6.(11分)新制氯水中含有多种粒子,某校化学研究性学习小组的同学为探究其性质,做了如下实验,请你帮助完成:
(1)HClO不稳定,见光易分解生成HCl和O2。请设计实验证明有O2生成__________________________________________________________________________________________________________________________ 。
(2)氯气能使湿润的红色布条褪色。对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能。请你设计实验,得出正确结论。
|
提出问题 |
收集资料 |
提出假设 |
验证假设 |
得出结论 |
|
氯水中何种物质能使湿润的红色布褪色? |
①氯气有强氧化性 ②氯气与冷水反应生成盐酸和次氯酸 ③次氯酸有强氧化性 |
①_____________ ____________ 。 ②_____________ ____________ 。 ③____________ _____________ 。 ④ H2O使布条褪色 |
实验1:把红色干布条放入充满氯气的集气瓶中,布条不褪色; 实验2:_______________ ______________。 实验3:把红色布条放在水里,布条不褪色。 |
__________ __________ __________ |
(3)平衡常数表明了封闭体系的可逆反应在给定的温度下进行的程度,对于同一个类型的反应,平衡常数越大,表明反应进行的程度越大。
H2CO3  HCO3- + H+ Ka1(H2CO3)
= c(HCO3-)·c(H+)/c(H2CO3) =
4.45×10-7
HCO3- + H+ Ka1(H2CO3)
= c(HCO3-)·c(H+)/c(H2CO3) =
4.45×10-7
HCO3- CO32- + H+
Ka2(H2CO3) = c(CO32-) ·c(H+)/ c(HCO3-) = 5.61×10-11
CO32- + H+
Ka2(H2CO3) = c(CO32-) ·c(H+)/ c(HCO3-) = 5.61×10-11
HClO  H+ + ClO- Ka(HClO)
= 2.95×10-8
H+ + ClO- Ka(HClO)
= 2.95×10-8
请依据以上碳酸和次氯酸的电离平衡常数,写出在下列条件下所发生反应的离子方程式:
①将少量的氯气通入到过量的碳酸钠溶液中_________________________ ;
②氯气和碳酸钠按照1∶1的比例恰好反应_______________________;
③将过量的氯气通入到少量的碳酸钠溶液___________________。
2008届高三化学实验题练习
5. (12分)我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3+CO2+H2O
(12分)我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3+CO2+H2O NH4HCO3 ; NH4HCO3+NaCl NaHCO3↓+NH4Cl ;2NaHCO3 Na2CO3+CO2↑+H2O
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是 (填字母标号)。
a.碳酸氢钠难溶于水 b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
① 一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。
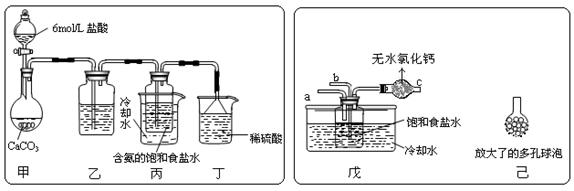
试回答下列有关问题:
 (Ⅰ)乙装置中的试剂是 ; (Ⅱ)丁装置中稀硫酸的作用是
;
(Ⅰ)乙装置中的试剂是 ; (Ⅱ)丁装置中稀硫酸的作用是
;
(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是 (填分离操作的名称)。
② 另一位同学用图中戊装置(其它装置未画出)进行实验。
(Ⅰ)实验时,须先从 管通入 气体,再从 管中通入 气体;
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是
(3)请你再写出一种实验室制取少量碳酸氢钠的方法:
4.锶(Sr)位于元素周期表的第5周期ⅡA族。碳酸锶大量用于生产彩色电视显像管的荧光屏玻璃。工业上常以天青石(主要成分为硫酸锶,含不溶性杂质)为原料,采用以下两种方法制取碳酸锶,进而制得多种锶的化合物。
方法一:将天青石粉碎后在1000℃-1200℃时与碳在还原气氛中反应制得硫化锶。向硫化锶溶液中通人CO2得到碳酸锶。
方法二:将天青石粉末与碳酸钠溶液的混合物在90℃时加热l-2 h,经过滤、洗涤,得到碳酸锶。
(1) 方法一将天青石粉碎的目的是__________________
__________________
。写出用碳还原天青石反应的化学方程式:_____________________________________。
(2) 方法二的反应能够发生,说明______________
____
。为了使该反应充分进行,还可以采取的措施是__________ 。
(3)两种方法中得到的碳酸锶纯度较高的是_______________(填“方法一”或“方法二”),理由是______________________________________________
。
(4)下列关于锶及其化合物的叙述中,正确的是___________。
A.离子半径:Ba2+>Sr2+>Ca2+ >Be2+ B.碱性:Ba(OH)2>Sr(OH)2>Ca(OH)2
C.SrCO3高温分解可以制取SrO D.SrCO3与HNO3溶液反应可制取Sr(NO3)2
3.2007年诺贝尔化学奖授予德国科学家格哈德·埃特尔,以表彰他在表面化学研究领域作出的开拓性贡献。(12分)
 (1)某校化学研究性学习小组的同学在技术人员的指导下,按下列
(1)某校化学研究性学习小组的同学在技术人员的指导下,按下列
流程探究不同催化剂对NH3还原NO反应的催化性能。
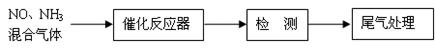
若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,
将经催化反应后的混合气体通过滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。为比较不同催化剂的催化性能,需要测量并记录的数据是 。
(2)在汽车的排气管上安装“催化转化器”(用铂、钯合金作催化剂),它的作用是使CO、NO反应生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧。
①写出CO与NO反应的化学方程式: ,该反应作氧化剂的物质是_________。
②用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g) 4NO(g)+CO2(g)+2H2O(g); ΔH1=-574
kJ·mol-1
CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(g); ΔH2
若1mol CH4还原NO2至N2,整个过程中放出的热量为867kJ,则ΔH2= 。
(3)①有人认为:该研究可以使氨的合成反应,在铁催化剂表面进行时的效率大大提高,从而使原料的转化率大大提高。请你应用化学基本理论对此观点进行评价:
。
②合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3,当催化剂中Fe2+与Fe3+的物质的量之比为1:2时,其催化活性最高,以Fe2O3为原料制备上述催化剂,可向其中加入适量炭粉,发生如下反应:2 Fe2O3十C
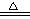 4FeO十CO2↑。为制得这种活性最高的催化剂,应向480g Fe2O3粉末中加入炭粉的质量为
g。
4FeO十CO2↑。为制得这种活性最高的催化剂,应向480g Fe2O3粉末中加入炭粉的质量为
g。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com