
题目列表(包括答案和解析)
23、(本题11分)根据下列框图(题23图)回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
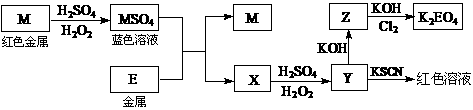
(1)M的名称 , X的化学式 ,Z的化学式 。
(2)写出M溶于稀H2SO4和H2O2混合液的化学方程式: 。
(3)某同学取X的溶液(已经置于空气一段时间),酸化后加入KI、淀粉溶液,变为蓝色。
写出与上述变化过程相关的离子方程式: 、 。
(4)写出Cl2将Z氧化为K2EO4的化学方程式: 。
22、(本题6分,每空2分)有一瓶澄清溶液, 可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO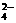 、CO
、CO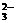 、NO
、NO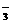 、Cl-、I-现进行如下实验:
、Cl-、I-现进行如下实验:
(1)测该溶液显强酸性;
(2)取样加少量四氯化碳和数滴新制氯水、CCl4层为紫红色;
(3)另取样滴加稀NaOH溶液, 使溶液变为碱性, 此过程无沉淀生成;
(4)取少量上述碱性溶液, 加Na2CO3溶液出现白色沉淀;
(5)将实验(3)中的碱性溶液加热, 有气体放出, 该气体能使湿红色石蕊试纸变蓝。
问:(1)原溶液中肯定存在的离子是 ;
(2)肯定不存在的离子是 ;
(3)不能确定是否存在的离子是 。
21、(本题6分,每空2分)今有①CH3COOH、②HCl、③H2SO4 三种溶液,用序号回答下列问题
(1)当它们的物质的量浓度相同时,其pH的由大到小排列是__________________。
(2)当它们pH相同时,其物质的量浓度的由大到小排列是_________________。
(3)中和同一烧碱溶液,需同浓度的三种酸溶液的体积关系为 _________________。
20、甲、乙均属于金属元素,下列事实能判断甲的金属性一定比乙强的是
①甲单质能于乙的盐溶液反应 ②甲、乙两元素原子的最外层电子数相同,且甲的原子半径小于乙 ③甲、乙两短周期元素原子的电子层数相同,且甲的原子序数小于乙 ④两单质和盐酸组成原电池,乙单质表面生成氢气 ⑤等物质的量的两种单质分别与足量氯气反应时,甲失去的电子数比乙多
A、①②③④⑤ B、只有③④ C、只有①③④ D、只有①③④⑤
Ⅱ卷 非选择题(60分)
19、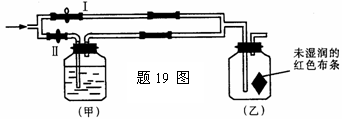 如右图(题19图)所示:若关闭Ⅱ阀打开Ⅰ阀,让一种含有氯气的气体经过乙瓶后,布条不褪色。若关闭Ⅰ阀,打开Ⅱ阀,再通入这种气体,通入乙瓶 ,布条褪色;甲瓶中所盛的试剂可能是
如右图(题19图)所示:若关闭Ⅱ阀打开Ⅰ阀,让一种含有氯气的气体经过乙瓶后,布条不褪色。若关闭Ⅰ阀,打开Ⅱ阀,再通入这种气体,通入乙瓶 ,布条褪色;甲瓶中所盛的试剂可能是
A、浓H2SO4 B、NaOH溶液
C、KI溶液 D、饱和NaCl溶液
18、下列的描述中不正确的是
A、常温下 ,pH=1的醋酸溶液中,醋酸分子的数目一定大于0.1mol
B、一定条件下的可逆反应,反应物的转化率不可能达到100%
C、沉淀转换的实质就是沉淀溶解平衡的移动,平衡一般向生成更难溶物质的方向移动
D、△H<0,△S>0的反应一定是自发进行的化学反应
17、工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g) Si(s)+4HCl(g); △H=+QKJ /mol(Q>0),某温度、压强下,
Si(s)+4HCl(g); △H=+QKJ /mol(Q>0),某温度、压强下,
将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
A、反应过程中,若压缩容器体积,增大压强能提高SiCl4的转化率
B、若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ
C、当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol/L的NaOH溶液恰好反应
D、反应至4 min时,若HCl浓度为0.12 mol/L,则H2的反应速率为0.03 mol/(L·min)
16、奥运吉祥物福娃外材为纯羊毛线,内充物为无毒的聚酯纤维,其结构简式为:
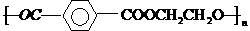
 ,下列说法不正确的是 ( )
,下列说法不正确的是 ( )


A、羊毛与聚酯纤维的化学成分不相同
B、聚酯纤维和羊毛在一定条件下均能水解
C、合成聚酯纤维的单体为对苯二甲酸和乙二醇
D、由单体合成聚酯纤维的反应属加聚反应
15、下列溶液中的Cl- 浓度与50 mL 1 mol/L MgCl2溶液中的Cl-浓度相等的是
A、150 mL 1mol/L NaCl 溶液 B、75 mL 2mol/L CaCl2 溶液
C、150 mL 2mol/L KCl 溶液 D、75 mL 1mol/L AlCl3 溶液
14、下列反应的离子方程式书写正确的是
A、小苏打溶液和甲酸溶液混合 HCO3-+H+=CO2↑+H2O
B、铝片放入NaOH溶液中 2OH-+Al=AlO2-+H2↑
C、次氯酸钙溶液中通入过量二氧化碳 Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO
D、氨水中通入少量二氧化硫 2NH3·H2O+SO2=2NH4++SO32-+H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com