
题目列表(包括答案和解析)
21. 硝酸工厂的尾气氮氧化合物若不加以处理排放到大气中,不仅会形成硝酸型酸雨,还可以形成光化学烟雾。因此必须对含有氮氧化合物的废气进行处理。
(1)用氢氧化钠溶液可以吸收废气中的氮氧化合物,反应的化学方程式为:
NO2 + NO + 2NaOH == 2NaNO2 + H2O
标出电子转移的方向和数目。在该反应中,每生成1 mol NaNO2、转移电子的数目为 。
(2)汽车尾气中含有NO和CO,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成N2和CO2。该反应的化学方程式为:
。
氧化剂是 ,还原剂是 。
20.
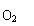
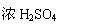
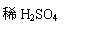 用铜和浓硫酸为原料制取硫酸铜时,可用下列两种方案:
用铜和浓硫酸为原料制取硫酸铜时,可用下列两种方案:
甲方案:Cu---→CuSO4 乙方案:Cu--→CuO---→CuSO4
写出甲方案的化学方程式:
这两种方案对比, 方案更好,理由是:
19. 请写出反应的化学方程式:
(1)用NaOH溶液吸收SO2气体:
(2)工业上采用接触法制硫酸,其中在接触室进行的反应是:
(3)铜与稀硝酸反应:
18. 利用氧化还原反应原理配平
NH3 + O2 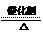 NO + H2O
NO + H2O
17. 浓硫酸在下列用途和现象中所表现的性质是
A、沸点高、难挥发 B、酸性 C、吸水性 D、脱水性 E、强氧化性
|
用途或现象 |
体现浓硫酸的性质 |
|
(1)浓硫酸使蓝矾变成白色 |
|
|
(2)浓硫酸使木条变黑 |
|
|
(3)浓硫酸制HCl |
|
|
(4)浓硫酸与铜片共热 |
|
|
(5)浓硫酸的木炭共热产生气体 |
|
16. 向100mL 18.4mol·L-1的浓硫酸溶液中加入足量的铜片,加热,经充分反应后,可得到SO2气体物质的量( )mol
A、等于0.92 B、小于0.92 C、大于0.92 D、等于1.84
15.
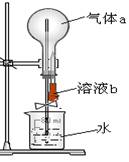 如右图所示,在干燥的圆底烧瓶中充满某气体a,胶头滴管中吸有少量液体b,当把溶液b挤进烧瓶后,打开止水夹不能形成“喷泉”的组合是( )
如右图所示,在干燥的圆底烧瓶中充满某气体a,胶头滴管中吸有少量液体b,当把溶液b挤进烧瓶后,打开止水夹不能形成“喷泉”的组合是( )
|
|
干燥气体a |
液体b |
|
A |
NH3 |
水 |
|
B |
HCl |
水 |
|
C |
CO2 |
NaOH溶液 |
|
D |
Cl2 |
饱和食盐水 |
14. 发射“神六”的运载火箭,其推进剂引燃后发生剧烈反应,产生大量高温无色气体(CO2、H2O、N2、NO)从火箭尾部喷出。但在发射现场看到火箭尾部喷出大量棕红色的气体,产生棕红色的气体的原因是( )
A、NO遇空气生成NO2
B、高温下N2遇空气生成NO2
C、CO2与N2反应生成CO和NO2
D、NO和H2O反应生成H2和NO2
13. 氨水显弱碱性的主要原因是( )
A、通常状况下,氨的溶解度不大 B、氨水中的NH3·H2O电离出少量OH-
C、溶于水的氨分子只有少量电离 D、氨本身的弱碱性
12. 常温下,下列各组气体能共存(即不发生反应)的是( )
A、NH3和HCl B、NH3和SO2 C、N2和O2 D、NO和O2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com