
题目列表(包括答案和解析)
19.(07海南卷)NaCl的晶胞如图,每个NaCl晶胞中含有的Na+离子和Cl-离子的数目分别是( )
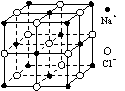

A.14,13 B. 1,1 C. 4,4 D. 6,6
18.(08海南卷)已知X、Y、Z三种元素组成的化合物是离子晶体,其晶胞如图所示,则下面表示该化合物的化学式正确的:
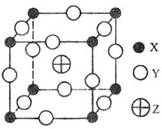
A.ZXY3 B.ZX2Y6 C.ZX4Y8 D.ZX8Y12
17.(04北京卷)近期《美国化学会志》报道,中国科学家以二氧化碳为碳源,金属钠为还原剂,在470℃、80Mpa下合成出金刚石,具有深远意义。下列说法不正确的是( )
A.由二氧化碳合成金刚石是化学变化 B.金刚石是碳的一种同位素
C.钠被氧化最终生成碳酸钠 D.金刚石中只含有非极性共价键
考点2 计算晶体的化学式
16.(04广东卷)X是核外电子数最少的元素,Y是地壳中含量最丰富的元素,Z在地壳中的含量仅次于Y,W可以形成自然界最硬的原子晶体。下列叙述错误的是( )
A.WX4是沼气的主要成分 B.固态X2Y是分子晶体
C.ZW是原子晶体 D.ZY2的水溶液俗称“水玻璃”
15.(04上海卷)有关晶体的下列说法中正确的是( )
A.晶体中分子间作用力越大,分子越稳定 B.原子晶体中共价键越强,熔点越高
C.冰熔化时水分子中共价键发生断裂 D.氯化钠熔化时离子键未被破坏
14.(05上海卷)下列说法错误的是( )
A.原子晶体中只存在非极性共价键
B.分子晶体的状态变化,只需克服分子间作用力
C.金属晶体通常具有导电、导热和良好的延展性
D.离子晶体在熔化状态下能导电
13.(05天津卷)下列说法正确的是( )
A.H与D,16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体;甲醇、乙二醇和丙三醇互为同系物
B.在SiO2晶体中,1个Si原子和2个O原子形成2个共价键
C.HI的相对分子质量大于HF,所以HI的沸点高于HF
D.由ⅠA族和ⅥA族元素形成的原子个数比为1∶1、电子总数为38的化合物,是含有共价键的离子型化合物
12.(06广东卷)下列物质性质的变化规律,与共价键的键能大小有关的是( )
A.F2、Cl2、Br2、I2的熔点、沸点逐渐升高
B.HF、HCl、HBr、HI的热稳定性依次减弱
C.金刚石的硬度、熔点、沸点都高于晶体硅
D.NaF、NaCl、NaBr、NaI的熔点依次降低
11.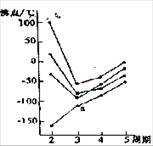 (06北京卷)右图中每条折线表示周期表ⅣA-ⅦA中
(06北京卷)右图中每条折线表示周期表ⅣA-ⅦA中
的某一族元素氢化物的沸点变化,每个小黑点代表一
种氢化物,其中a点代表的是( )
A.H2S B.HCl
C.PH3 D.SiH4
10.(06上海卷)根据相关化学原理,下列判断正确的是( )
A.若X是原子晶体,Y是分子晶体,则熔点:X<Y
B.若A2十2D-=2A-十D2,则氧化性:D2>A2
C.若R2-和M+的电子层结构相同,则原子序数:R>M
D.若弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的碱性:NaA<NaB
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com