
题目列表(包括答案和解析)
3.(08宁夏卷)短周期元素E的氯化物ECln的熔点为-78℃,沸点为59℃;若0.2molECln与足量的AgNO3溶液完全反应后可以得到57.4g的AgCl沉淀。下列判断错误的是( )
A.E是一种非金属元素 B.在ECln中E与Cl之间形成共价键
C.E的一种氧化物为EO D.E位于元素周期表的IVA族
2.(08广东卷)元素X、Y和Z可结合形成化合物XYZ3;X、Y和Z的原子序数之和为26;Y和Z在同一周期。下列有关推测正确的是( )
A.XYZ3是一种可溶于水的酸,且X与Y可形成共价化合物XY
B.XYZ3是一种微溶于水的盐,且X与Z可形成离子化合物XZ
C.XYZ3是一种易溶于水的盐,且Y与Z可形成离子化合物YZ
D.XYZ3是一种离子化合物,且Y与Z可形成离子化合物YZ3
1.(08全国Ⅰ卷)下列各组给定原子序数的元素,不能形成原子数之比为1∶1稳定化合物的是( )
A.3和17 B.1和8 C.1和6 D.7和12
26.(新课标高考题)(08山东卷)氮是地球上极为丰富的元素。
(1)Li3N晶体中氮以N3-存在,基态N3-的电子排布式为 。
(2)N≡N的键能为942 kJ·mol-1,N-N单键的键能为247 kJ·mol-3,计算说明N2中的
键比
键稳定(填“ ”“
”“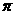 ”)。
”)。
(3)(CH3)3NH+和AlCl-4可形成离子液体。离子液体由阴、阳离子组成,熔点低于100℃,其挥发性一般比有机溶剂 (填“大”或“小”),可用作 (填代号)。
 a、助燃剂
b、“绿色”溶剂
a、助燃剂
b、“绿色”溶剂
c、复合材料 d、绝热材料
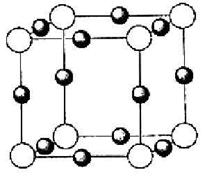
(4)X*中所有电子正好充满K、L、M三个电子层,它与N3-形成
的晶体结构如图所示。X的元素符号是 ,与同一个
N3-相连的X*有 个。
25.(新课标高考题)(08上海卷)(A)四种短周期元素的性质或结构信息如下表,请根据信息回答下列问题:

(1)B元素在周期表中的位置是_________________________,写出A原子的电子排布式__________________。
(2)写出C单质与水反应的化学方程式____________________________________________。A与C形成的化合物溶于水后,溶液的pH__________7(填“大于”、“等于”或“小于”)。
(3)D元素最高价氧化物晶体的硬度________(填“大”、“小”),其理由是____________________________。
(4)A、B两元素非金属性较强的是(写元素符号)__________。写出能证明这一结论的一个实验事实_____________________________________________________。
24.(07天津卷)U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)V的单质分子的结构式为______________;XW的电子式为__________________;Z元素在周期表中的位置是_________。
(2)U元素形成的同素异形体的晶体类型可能是(填序号)________________。
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)__________;V、W的氢化物分子结合H+能力较强的是(写化学式)__________,用一个离子方程式加以证明___________________________________。
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为__________________。
由此可知VW和YW2还原性较强的是(写化学式)____________。
23.(07重庆卷) a、b、c、d、e是短周期元素,周期表中a与b、b与c相邻;a与e的最外层电子数之比为2:3,b的最外层电子数比e的最外层电子数少1个;常见化合物d2c2与水反应生成c的单质,且溶液使酚酞试液变红。
(1)e的元素符号是__________。
(2)a、b、c的氢化物稳定性顺序为(用分子式表示)__________________;b的氢化物和b的最高价氧化物的水化物反应生成Z,则Z中的化学键类型为__________________,Z的晶体类型为_____________;ab-离子的电子式为____________。
(3)由a、c、d形成化合物的水溶液显碱性,其原因是(用离子方程式表示)_____________________________________。
(4)一定量的d2c2与ac2反应后的固体物质,恰好与0.8 mol稀盐酸溶液完全反应,并收集到0.25 mol气体,则用物质的量表示该固体物质的组成为__________________、___________________。
22.(08四川卷)D、E、X、Y、Z是周期表中的前20号元素,且原子序数逐渐增大,它们的最简单氢化物分子的空间结构依次是正四面体、三角锥形、正四面体、角形(V形)、直线型,回答下列问题:
(1)Y的最高价氧化物的化学式为______________。
(2)上述5种元素中,能形成酸性最强的含氧酸的元素是____________,写出该元素的任意3种含氧酸的化学式:_______________________。
(3)D和形成的化合物,其分子的空间构型为________________。
(4)D和X形成的化合物,其化学键类型属_______________,其晶体类型属_____________________。
(5)金属镁和E的单质在高温下反应得到的产物是__________,此产物与水反应生成两种碱,该反应的化学方程式是___________________________。
(6)试比较D和X的最高价氧化物熔点的高低并说明理由_______________________________________。
21.(05江苏卷)通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
|
化学键 |
Si-O |
Si-Cl |
H-H |
H-Cl |
Si-Si |
Si-C |
|
键能 / kJ·mol-1 |
460 |
360 |
436 |
431 |
176 |
347 |
 请回答下列问题:
请回答下列问题:
(1)比较下列两组物质的熔点高低(填“>”或“<”)
SiC Si;SiCl4 SiO2
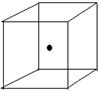
(2)右图立方体中心的“●”表示硅晶体中的一个原子,
请在立方体的顶点用“●”表示出与之紧邻的硅原子。
 (3)工业上高纯硅可通过下列反应制取:
(3)工业上高纯硅可通过下列反应制取:
SiCl4(g)+2H2(g) Si(s)+4HCl(g)
该反应的反应热△H=_____________kJ / mol
考点3 综合应用
20. (06江苏卷)下列关于晶体的说法一定正确的是( )
(06江苏卷)下列关于晶体的说法一定正确的是( )
A.分子晶体中都存在共价键
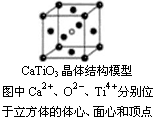
B.CaTiO3晶体中每个Ti4+和12个O2-相紧邻
C.SiO2晶体中每个硅原子与两个氧原子以共价键相结合
D.金属晶体的熔点都比分子晶体的熔点高
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com