
题目列表(包括答案和解析)
18.FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、NO和H2O,当NO2、NO的物质的量之比为1:1时,实际参加反应的FeS与HNO3的物质的量之比为
( )
A.2:9 B.2:11 C.2:15 D.2:5
第Ⅱ卷(非选择题,共66分)
17.20℃时。饱和KC1溶液的密度为1.174g·cm-3,物质的量浓度为4.0mol·L-1,则下列说法中不正确的是 ( )
A.25℃时,饱和KC1溶液的浓度大于4.0mol·L-1
B.此溶液中KC1的质量分数为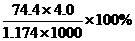
C.20℃时,密度小于1.174g·cm-3的KC1溶液是不饱和溶液
D.将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174g·cm-3
16.已知反应:①101kPa时,2C(s)+O2(g)=2CO(g); △H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(1);△H=-57.3kJ/mol
③红磷的化学式为P,白磷的化学式为P4,已知
P4(s)+5O2(g)=P4O10(s);△H=-3093.5kJ/mol
4P(s)+5O2(g)=P4O10(s);△H=-2954.0kJ/mol
下列结论正确的是 ( )
A.由于红磷转化为白磷是放热反应,等质量的红磷能量比白磷低
B.碳的燃烧热大于110.5kJ/mol
C.稀硫酸与稀NaOH溶液反应的中和热△H=57.3kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
15.实验室用固态不纯氯化钠(含少量NH4HCO3和Na2SO4杂质)制取纯净氯化钠溶液。下列操作可供选用:①逐滴加入稀盐酸,调pH值 为5;②煮沸;③加蒸馏水溶解;④加热至不再产生气体为止;⑤加入稍过量的NaCO3溶液;⑥加入稍过量的BaC12溶液;⑦过滤。上述实验操作的正确顺序应是 ( )
A.①②⑤⑥⑦③④ B.③④⑥⑤⑦①②
C.④③⑥⑤⑦①② D.④③⑤⑥⑦②①
14.40℃时,等质量的两份饱和石灰水,一份冷却至10℃,另一份加少量CaO并保持温度仍为40℃,这两种情况都不改变的是 ( )
A.Ca(OH)2的溶解度 B.溶液的质量
C.溶质的质量分数 D.溶液中Ca2+数目
13.有甲、乙两溶液,各含下列14种离子中的7种:A13+、C1-、Na+、K+、NO3-、OH-、S2-、MnO4-、Fe3+、A1O2-、CO32-、NH4+、SO42-、H+。已知两溶液所含离子各不相同,甲溶液里只有2种阳离子,则乙溶液里的阴离子应该是 ( )
A.OH-、S2-、CO32- B.MnO4-、SO42-、NO3-
C.C1-、NO3-、SO42- D.A1O2-、MnO4-、SO42-
12.下列过程溶液可能会变浑浊的有 ( )
①钠投入饱和食盐水中;
②少量钠投入饱和NaHCO3溶液中;
③过量的CO2通入饱和Na2CO3溶液中;
④过量的CO2通入CaC12溶液中;
⑤足量的BaC12溶液加入NaHCO3溶液中
A.①② B.①③ C.①③④⑤ D.①②③④⑤
11.下列离子方程式正确的是 ( )
A.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O
B.酸酸钠的水解反应CH3COO-+H3O+=CH3COOH+H2O
C.Mg(HCO3)2溶液中加入过量石灰水:
Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓
D.向100mL 0.1mol/L 的FeBr2溶液中通入0.012molC12:
10Fe2++14Br-+12C12=10Fe3++7Br2+24C1-
10.NA代表阿伏加德罗常数,下列说法正确的是 ( )
A.标准状况下,22.4LCHC13中含有氯原子数目为3NA
B.7gCnH2n中含有的氢原子数目为NA
C.18gD2O中含有的质子数目为10NA
D.通常状况下 33.6L氯气与27g铝充分反应,转移电子数为3NA
9.下列离子方程式中,只能表示一个化学反应的是 ( )
①CO32-+2H+ CO2↑+H2O ②Ba2++2OH-+2H++SO42- BaSO4↓+2H2O
③Ag++C1-=AgC1↓ ④Fe+Cu2+ Fe2++Cu ⑤C12+H2O H++C1-+HC1O
A.①③ B.②④ C.②⑤ D.只有⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com