
题目列表(包括答案和解析)
8.有三种不同取代基-X,-Y,-Z,当它们同时取代苯分子中的3个氢原子,取代产物有
A.4种 B.6种 C.10种 D.14种
7.制印刷电路时常用氯化铁作腐蚀液,有关反应为2FeCl3 + Cu =2FeCl2 + CuCl2。向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,烧杯中不可能出现的是
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
6.在pH值都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH- 离子浓度分别为A摩/升与B摩/升,则A和B关系为
A.A>B B.A=10-4 B C.B=10-4 A D.A=B
5.溶质相同、质量分数为a%和b%的两份溶液质量分别为mg、ng,将两份溶液混合并蒸发去xg水,所得溶液的物质的量浓度为cmol/L。欲求溶质的摩尔质量,仍缺少一个数据,该数据是
A.蒸发后所得溶液的密度(ρ) B.混合前两份溶液的物质的量浓度(c)
C.蒸发前混合液的体积(V) D.溶质的溶解度(S)
4.碱金属与卤素所形成的化合物大都具有的性质是① 高沸点 ② 能溶于水 ③ 水溶液能导电 ④ 低熔点 ⑤ 熔融状态不导电
A.①②③ B.③④⑤ C.①④⑤ D.②③⑤
3.一定条件下,2CO(g) + O2(g) = 2CO2(g);⊿H=-566 kJ·mol-1;CH4(g)+2O2(g)=CO2(g)+2H2O(l);
⊿H=-890 kJ·mol-1,则1molCO和3molCH4组成的混合气体在上述条件下完全燃烧放出的热量为
A.2912 kJ B.2953 kJ C.3236 kJ D.3836 kJ
2.R、X、Y和Z是四种元素,其常见化合价均为+2价,且X2+与单质R不反应;X2+ + Z=X + Z2+;Z2+ + Y=Z + Y2+。这四种离子被还原成0价时表现的氧化性大小符合
A.R2+>X2+>Z2+>Y2+ B.X2+ >R2+ >Y2+>Z2+ C.Y2+>Z2+>R2+>X2+ D.Z2+>X2+>R2+>Y2+
1.某物质经分析,只含一种元素,则此物质
A.一定是一种单质 B.一定是纯净物
C.一定是混合物 D.可能是纯净物,也可能是混合物
36.(5分)溶液中含有Fe2+:0.5mol/L×0.2L=0.1mol
设Fe2(SO4)3反应消耗铁的物质的量为x,与CuSO4反应消耗铁的物质的量为y
Fe+Fe2(SO4)3=3FeSO4 Fe+CuSO4=FeSO4+Cu
1mol 1mol 3mol 1mol 1mol 1mol 1mol
xmol xmol 3xmol ymol ymol ymol ymol
可得:3x+y=0.1mol 6g-56x+8y=5.2g
解得x=0.02mol y=0.04mol
故得:生成铜质量为0.04mol×64g/mol=2.56g
原溶液中Fe2(SO4)3的物质的量浓度为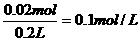
答:(1)反应后生成铜的质量为2.56g。(2)原溶液中Fe2(SO4)3的物质的量浓度为0.1mol/L。
35.(8分)(1)B 3 (2)氢 (3)IVA (4)位置略 Cl->Mg2+>Al3+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com