
题目列表(包括答案和解析)
1.常见气体的实验室制法是高考的重点内容,它包括所用试剂、反应原理、仪器装置和收集方法。
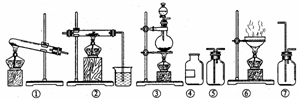 中学教材中按反应物的状态及反应条件可将气体制备分为五组:
中学教材中按反应物的状态及反应条件可将气体制备分为五组:

 (1)固+固 气组:有O2、NH3等;
(1)固+固 气组:有O2、NH3等;

 (2)固+液 气组:有H2、O2、CO2、NH3、H2S、SO2、NO2、C2H2等;
(2)固+液 气组:有H2、O2、CO2、NH3、H2S、SO2、NO2、C2H2等;
(3)固+液 气组:有Cl2、HCl、NO等;
(4)液+液 气组:有C2H4和CO等。
(5)能用启普发生器制取的气体有:H2、CO2、H2S等。
要求熟练掌握以上各种气体的制取所需药品、化学原理、装置简图、净化方法、检验和操作注意事项。
9.(1)第②种方法比较节约试剂。从化学方程式看出,同样是制备2 mol 的Al(OH)3,方法①所需原料为:2 mol Al,3 mol H2SO4,6 mol NaOH;而方法②所需原料为:2 mol Al,1 mol H2SO4,2 mol NaOH。
(2)① 2Al + 3H2SO4==Al2(SO4)3 + 3H2↑
② 2Al + 2H2O + 2NaOH==2NaAlO2 + 3H2↑
③ Al2(SO4)3+ 6NaAlO2 + 12H2O==8Al(OH)3↓+ 3Na2SO4
由方程式看出,制备8mol 的Al(OH)3,所需原料为:8
mol Al,3 mol H2SO4,6
mol NaOH。相当于制备2mol
Al(OH)3,所需量为:2 mol Al,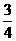 mol H2SO4,
mol H2SO4,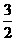 mol NaOH,其用量为最少。
mol NaOH,其用量为最少。
8.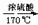 (1)CH3CH2OH CH2=CH2↑+H2O
(1)CH3CH2OH CH2=CH2↑+H2O
CH2=CH2 +Br2→CH2 Br CH2 Br
(2)b中水面会下降,玻璃管中的水面会上升,甚至溢出。
(3)除去乙烯中带出的酸性气体或答二氧化碳、二氧化硫。
(4)①乙烯发生(或通过液溴)速度过快 ②实验过程中,乙烯和浓硫酸的混合液没有迅速达到170℃(或写“控温不当”也可以)
7.(1)A、E(或F)、C
(2)2Na2O2+2H2O=4NaOH+O2↑或2H2O2 = 2H2O+O2↑
(3)取带火星的木条置于集气瓶口,木条复燃,证明已收集满
(4)①C2H2 CaC2和水(或饱和食盐水)
②NH3 浓氨水和CaO
③SO2 Na2SO3和硫酸
④HCl 浓硫酸和浓盐酸
1.C 2.B 3.B 4.D 5.D
讲析:3.观察双球洗气管中的液面,再分析表格中四种气体的溶解度数据,可知是极易溶于水的气体表现的性质。4.制备乙烯用浓硫酸和乙醇;稀硝酸具有强氧化性,与锌反应不可能制得H2;大理石与稀硫酸反应生成的CaSO4微溶,覆盖在大理石的表面,阻止反应继续进行;浓硝酸具有强氧化性,将Na2SO3氧化,不能制得SO2。5.全面分析气体的干燥、收集和尾气处理装置,只有NH3符合。
3.(1)CaC2+2H2O→C2H2↑+ Ca(OH)2
HC≡CH+Br2→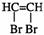
(或HC≡CH+2Br2→ )
)
(2)不能 a、c
(3)H2S Br2+H2S = S↓+2HBr
(4) c b
(CuSO4溶液) (CuSO4溶液)
(5)如若发生取代反应,必定生成HBr,溶液酸性将会明显增强,故可用pH试纸验证。
检测提高
2.C 讲析:由铜元素守恒,可知C正确。H2还原CuO的实验操作要求是:先通入H2排空气,加热反应后得到的Cu要在H2流中冷却,所需H2比反应消耗的H2要多,则A、B、D不正确。
1.(1)①③⑤;②④⑦⑧ (2)①③⑥,A
(3)①②③④⑥⑧,B (4)⑥
讲析:气体的收集方法有:①向上排空气法(收集密度比空气大的气体);②向下排空气法(收集密度比空气小的气体);③排水集气法(收集难溶于水的气体)。
利用两导气管的长短可判断采用何种收集方法。
9.今用铝、稀硫酸和氢氧化钠溶液为原料,实验室制备一定量的氢氧化铝。可分别采用如下化学方程式所表示的两种方法:
①2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑
Al2(SO4)3 + 6NaOH = 2Al(OH)3↓+ 3Na2SO4
②2Al + 2NaOH + 2H2O==2NaAlO2 + 3H2↑
2NaAlO2 + H2SO4 + 2H2O==2Al(OH)3↓+ Na2SO4
(1)请问上述哪一种方法比较节约试剂?(提示:试从每生产2 mol Al(OH)3所耗费的试剂用量予以说明。)
(2)原料相同,请设计一种更为节约试剂的方法(以化学方程式表示,并说明其可以最节约试剂的根据)。
答案分析:
纠错训练
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com