
题目列表(包括答案和解析)
7.为方便某些化学计算,有人将98%浓硫酸表示成下列形式,其中合理的是 ( )
A.H2SO4·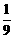 B.H2SO4 ·H2O C.H2SO4·SO3 D.SO3·
B.H2SO4 ·H2O C.H2SO4·SO3 D.SO3·
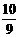 H2O
H2O
6.将N02、NH3、O2混合气22.4L通过稀硫酸后,溶液质量增加了26.7g,气体体积缩小为4.48L.(气体体积均在标况下测定)剩余气体能使带火星的木条着火,则混合气体的平均分子量为 ( )
A.28.1 B.30.2 C.33.1 D.34.0
5.由X、Y两元素组成的气态化合物XY4,在一定条件下完全分解为A、B两种气体物质,己知标准状况下20mLXY4分解可产生标准状况下30mL A气体(化学式为Y2)和10mL B气体,则B的化学式为 ( )
A.X2 B.Y2X2 C.XY2 D.X2Y4
4.由CO2、H2和CO组成的混合气在同温同压下与氮气的密度相同。则该混合气体中CO2、H2和CO的体积比为 ( )
A.29:8:13 B.22:l:14 C.13:8:29 D.26:16:57
3.由钾和氧组成的某种离子晶体含钾的质量分数是78/126,其阴离子只有过氧离子(O22-)和超氧离子(O2-)两种。在此晶体中,过氧离子和超氧离子的物质的量之比为 ( )
A.2:l B.1:l C.1:2 D.1:3
2.下列各组中两种气体的分子数一定相等的是 ( )
A.温度相同、体积相同的O2和N2 B.质量相等、密度不等的N2和C2H4
C.体积相同、密度相等的CO和C2H4 D.压强相同、体积相同的O2和H2
1.质量相等的两份气体样品,一份是CO,另一份是CO2,这两份气体样品中,CO与CO2所含氧原子的原子个数之比是 ( )
A.1:2 B.1:4 C.11:14 D.1l:28
7.某温度(t℃)时,水的离子积为Kw=1×10-13,则该温度(选填大于、小于或等于)
25℃,其理由是
。
若将此温度下pH=11的苛性钠溶液aL与pH=1的稀硫酸bL混合(设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两溶液的体积比:
(1)若所得混合液为中性,则a:b= : ;此溶液中各种离子的浓度由大到小排列顺序是 。
(2)若所得混合液的pH=2,则a:b= : ;此溶液中各种离子的浓度由大到小排列顺序是 。
6.在长期载人太空飞行的宇航器中,每个宇航员平均每天需要消耗0.9 kg氧气,呼出1.0 kg CO2,为保持飞船内空气的成分稳定,宇航科学家进行了大量的科学探索,有的科学家根据电解原理设计了飞船内空气更新实验系统,该系统结构示意图如下

(1)管道①的作用是飞船座舱中含较多二氧化碳后潮湿空气通入“电化学二氧化碳”处理系统的N极室,该电极反应可以使二氧化碳不断被吸收,其反应方程式为: ,其电解产物吸收二氧化碳的离子方程式为 ,在N极吸收二氧化碳后形成的离子会通过隔膜进入M极室,通过M极的电极反应可以使二氧化碳从电解溶液中释放出来,并保持系统内pH不变,该电极反应式为 。二氧化碳逸出的离子方程式为 。
(2)管道②的作用是将处理后的空气混入“电解水系统产生的新鲜氧气”,然后通入飞船座舱内供宇航员呼吸用。在电解水系统中,Y为 (填阴极、阳极)。X极的电极反应式 。
(3)逸出的二氧化碳没有排出飞船外,而是通过管道③进入“二氧化碳还原系统”,在该系统内,二氧化碳跟氢气在一定条件下反应,其产物有甲烷等气体。请评价这样处理的重要意义。
5.银器皿日久表面逐渐变黑,这是由于生成硫化银。有人设计用原电池原理加以除去,其处理方法为:将一定浓度的食盐水放入一铝制容器中,再将变黑银器浸入溶液中,放置一段时间后,黑色褪去而银不会损失,试回答
(1)原电池的正极反应为: 负极反应为:
(2)在反应过程中有臭鸡蛋气味的气体产生,写出电池的总反应方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com