
题目列表(包括答案和解析)
7.在100mL 0.10 mol·L-1的AgNO3溶液中加入100mL溶有0.01mol BaCl2的溶液,再加入100mL溶有0.01mol CuS04·5H20的溶液,充分反应。下列说法中正确的是 ( )
A.最终得到白色沉淀和无色溶液
B.最终得到的白色沉淀是等物质的量的两种化合物的混合物
C.在最终得到的溶液中Cl-的物质的量为0.02mol
D.在最终得到的溶液中,Cu2+的物质的量浓度为0.01 mol·L-1
6.有4.8g CuO、Fe2O3混合物与充足的CO于加热条件充分反应,反应后全部气体用0.6mol·L-1 Ba(OH)2溶液100mL处理,有白色沉淀生成。又知反应后,气体质量为3.52g,下列有关叙述中正却的是 ( )
A.原混合物中CuO与Fe2O3物质的量的比为l:l
B.生成的CO2已被Ba(OH)2溶液完全吸收、Ba2+沉淀完全
C.在吸收CO2后的Ba(OH)2溶液中可能有Ba(HCO3)2
D.原混合物中CuO与Fe2O3的质量比为2:1
5.铜和镁的合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只产生4480mL的NO2气体和336mL的N2O4气体(都已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为 ( )
A.9.02g B.8.51g C.8.26g D.7.04g
4.在外界提供相同电量的条件下,Cu2+或Ag+分别按Cu2++2e-→Cu或Ag++e-→Ag在电极上放电,若析出铜的质量为1.92g,财析出银的质量为 ( )
A.1.62g B.6.48g C.3.24g D.12.96g
3.20mL浓度为0.05mol·L-1的含Mn+离子的溶液,恰好把15mL的浓度为0.1mol·L-1的含S2-溶液中的S2-离子全部沉淀,则n的值是 ( )
A.4 B.3 C.2 D.1
2.A、B、C、D都是含碳、氢、氧的单官能团化合物,A水解得B和C,B氧化可以得到C或D,D氧化也得到C。若M(X)表示X的摩尔质量,则下式中正确的是 ( )
A.M(A)=M(B)+M(C) B.2M(D)=M(B)+M(C) C.M(B)<M(D)<M(C) D.M(D)<M(B)<M(C)
1.下图中横坐标表示完全燃烧时耗用可燃气体X(X=A、B、C)的物质的量n(X),纵坐标表示消耗O2的物质的量n(O2),A、B是两种可燃性气体,C是A和B的混合气体,则C中n(A):n(B)为 ( )
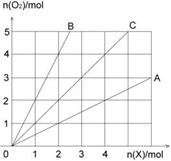 A.2:l B.1:2 C.1:1 D.任意比
A.2:l B.1:2 C.1:1 D.任意比
20.18.4g的NaOH和NaHCO3固体混合物,在密闭容器中加热到约250℃,经充分反应排出气体、冷却,称得剩余固体质量为16.6g(13.5g)。试计算原混合物中NaOH的质量分数?
Ⅳ综合计算
19.12g含有2种化合物(由常见主族的短周期元素组成)的白色固体与过量的盐酸,放出2.94L某种气体(标准状况),气体密度为同温同压下空气密度的1.52倍;剩余的不溶性残渣含氧53.3%,既不溶于水常温下又不易与稀碱溶液反应。通过计算分析这两种化合物可能是什么物质?(提示:此题为开放性试题,答案不止一种。请至少分析出两组合理的正确答案)
18.在空气中充分灼烧铜和硝酸铜的混合物,冷却后所得固体物质的质量和原混合物质的质量相同,求原混合物质中硝酸铜的质量分数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com