
题目列表(包括答案和解析)
1.化学与生产、生活、社会密切相关。下列有关说法中不正确的是
A.2008年北京奥运会开幕式上的“脚印”等焰火让全世界为之欢呼、倾倒,这主要是利用了化学中“焰色反应”的有关知识。
B.神七宇航员所穿航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料。
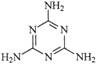 C.三鹿毒奶粉中的三聚氰胺是一种“伪蛋白”,其分子结构如右图所
C.三鹿毒奶粉中的三聚氰胺是一种“伪蛋白”,其分子结构如右图所
示,其化学式为C3H6N6。
D.2008年诺贝尔化学奖被授予研究“绿色荧光蛋白质”的美籍华裔
科学家钱永健等人。蛋白质都是由氨基酸形成的不可降解的高分子化合物,其水溶液有丁达尔效应。
(二) 下列实验操作或叙述正确的是 (填写编号,多选扣分)
①不宜用瓷坩埚灼烧氢氧化钠或碳酸钠固体;
②为了提高纯锌与稀硫酸反应的速率,可向稀硫酸中滴入几滴CuSO4溶液;
③用蒸馏水润湿的pH试纸测定溶液的pH一定有误差;
④向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,可以制得Fe(OH)3胶体;
⑤配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸;
⑥铵根离子检验时用湿润蓝色石蕊试纸;
⑦亚硫酸钠与浓硫酸反应制备SO2;
⑧往某溶液中加入BaCl2溶液产生白色沉淀,加稀硝酸沉淀不溶解,则溶液中一定有硫酸根离子.
29.将12.8克铜与一定量的浓硝酸反应,铜耗完时,共产生5.6升气体(标准状况)..
(1)产生气体的成份和物质的量分别是多少?
26.(16分)( l )右边曲线分别表示元素的某种性质与核电荷数的关系(Z 为核电荷数,Y为元素的有关性质)。把与下面元素有关的性质相符的曲线标号(a、b、c、d )填入相应的空格中:
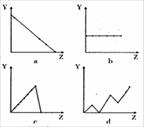 ① IIA 族元素的最外层电子数___________
① IIA 族元素的最外层电子数___________
② 第3 周期元素的最高化合价______
③ F-、Na+、Mg2+、Al3+的离子半径___________
( 2 )元素 X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。己知 Y 元素原子最外层电子数与核外电子总数之比为 3 : 4 ; M 元素原子的最外层电子数与电子层数之比为 4 : 3 ; N-、Z+、X+半径逐渐减小;化合物 XN 常温下为气体。据此回答:
① N 在周期表中的位置____________ ,N的最高价氧化物的水化物的化学式为_______________。
② 化合物 A、B 均为由上述五种元素中的任意三种组成的强电解质,且两种物质水溶液酸碱性相同,组成元素的原子数目比均为 1 : 1 : 1 , A 溶液中水的电离程度比 B 溶液中水的电离程度小,则化合物 A 中的化学键类型为__________________________,B 的化学式为_________________________________。
③ 工业上制取单质 M 的化学方程式为______________________________________。
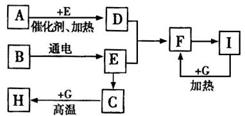
27、(10分)右图是中学化学中常见物质间的反应转化关系,其中部分产物已略去。常温下,G为固体单质,B、I液体,其余都为气体。A为化合物,I的浓溶液与G在加热条件下生成F、B和C,H可用作工业冶炼金属的还原剂。
试回答下列问题
(1)写出下列物质的化学式:A ,C 。
(2)A分子的结构呈 形。
(3)写出A→D的化学方程式
(4)写出G和I的浓溶液反应的化学方程式 。
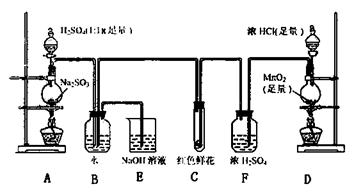 28.(20分)(一) 某学生为了测定部分变质的Na2SO3样品的纯度,设计了如下实验:
28.(20分)(一) 某学生为了测定部分变质的Na2SO3样品的纯度,设计了如下实验:
请回答下列问题:
(1)写出A装置中玻璃仪器的名称:酒精灯、 。
(2)实验开始后,写出B中反应的离子方程式 。
 (3)C中的现象是
,E装置的作用是
。
(3)C中的现象是
,E装置的作用是
。
(4)写出D中反应的离子方程式___________________
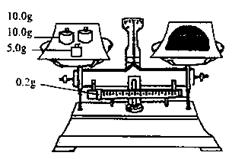
(5)按右图所示称取一定量的Na2SO3样品放入A
装置的烧瓶中,滴入足量的H2SO4完全反应。
然后将B中完全反应后的溶液与足量的BaCl2
溶液反应,过滤、洗涤、干燥,得白色沉淀23.3g
,则原样品中Na2SO3的纯度为
(精确到0.1%)。
(6)在过滤沉淀时若过滤液出现浑浊,则必须要重
复 操作,若该学生没有重复该操作则测定的结果将 (填“偏高”、“偏低”或“无影响”)。
(7)要使测定结果准确,第一:装置气密性必须良好;第二:应先点燃 处酒精灯(填装置字母)。
25.用98%的浓H2SO4(密度为1.84g/mL)1mol·L-1的H2SO4100mL,配制过程中可能用下到列仪器:
①100mL量筒;②10mL量筒;③50mL烧杯;④托盘天平;⑤100mL容量瓶;⑥胶头滴管;⑦玻璃棒。按使用的先后顺序排列正确的是
A.②⑥③⑦⑤ B.④③⑤⑦⑥ C.①③⑦⑤⑥ D.②⑤⑦⑥
第Ⅱ卷(非选择题,共55分)
24.下列有关能量转换的说法正确的是
A.煤燃烧是热能转化为化学能的过程
B.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能
C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程
23.下表为四种溶液的溶质质量分数和物质的量浓度的数值
|
溶液 |
KOH |
HNO3 |
CH3COOH |
HCl |
|
溶质质量分数ω(%) |
56 |
63 |
60 |
36.5 |
|
物质的量浓度c(mol/L) |
14.3 |
13.8 |
10.6 |
11.8 |
根据表中数据判断上述四种溶液中的密度最小的是
A.HCl B.HNO3 C.CH3COOH D.KOH
22.同温同压下,在3支相同体积的试管中分别充有等体积混合的2种气体,它们是①NO和NO2,②NO和O2,③NH3和N2。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积分别为V1、V2、V3,则下列关系正确的是
A V1>V2>V3 B V1>V3>V2 C V2>V3>V1 D V3>V1>V2
21.为确定下列置于空气中的物质是否变质,所选检验试剂(括号内物质)不能达到目的的是
A.HCHO溶液(石蕊试液) B.Na2SO3溶液(BaCl2)C.KI(淀粉溶液) D.FeCl2溶液(KSCN)
20.设NA表示阿伏加德罗常数,下列说法正确的是
A.在标准状况下,1molSO3的体积约为22.4L
B.10g重水(D2O)与2.3g钠反应生成气体的分子数为0.25NA
C.1L 1mol/LCH3COONa溶液中含有NA个CH3COO-
D.42gC2H4和C3H6的混合物中一定含有6NA个氢原子
19.已知R2+核内共有N个中子,R的质量数为A,确定mgR2+中含有电子的物质的量为
A.m(A-N)/A mol B.m(A-N+2)/ A mol
C.m(A-N-2)/ A mol D.核内中子数的总质量小于质子总质量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com