
题目列表(包括答案和解析)
30.(6分)用惰性电极电解NaCl与NaHCO3混合溶液,测得
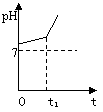 溶液pH变化如下图所示。
溶液pH变化如下图所示。
① 在0→t1时间内,两个电极上的电极反应式为:
阳极 ;
阴极 。
②用离子方程式表明0→t1时间内,溶液pH升高比较缓
慢的原因:
。
29.(4分)回答下列问题:
(1)保持恒温,向pH=6的蒸馏水中加入2.3g金属钠,充分反应后,再加蒸馏水稀释到1L,所得溶液的pH= 。
(2)以惰性电极电解CuSO4溶液。若阳极上产生气体的物质的量为0.01mol,则阴极上析
出Cu的质量为__________________________。 ..................
28.(10分)现有pH=2的醋酸溶液甲和pH=2的盐酸乙,请根据下列操作回答问题:
(1)取10 mL的甲溶液,加入等体积的水,醋酸的电离平衡 移动(填“向左”.“向右”或“不”);另取10 mL的甲溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/ c(CH3COOH)的比值将 (填“增大”.“减小”或“无法确定”)。
(2)相同条件下,取等体积的甲.乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为:pH(甲) pH(乙)(填“大于”.“小于”或“等于”)。
(3)各取25mL的甲.乙两溶液,分别用等浓度的NaOH溶液中和至pH=7,则消耗的NaOH溶液的体积大小关系为:V(甲) V(乙) (填“大于”.“小于”或“等于”)。
(4)取25 mL甲溶液,加入等体积pH=12的NaOH溶液,反应后溶液中c(Na+). c(CH3COO-)的大小关系为:c(Na+) c(CH3COO-)(填“大于”.“小于”或“等于” )。
27.在100mLCaCl2和盐酸的混合液中加入
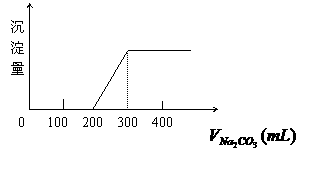
Na2CO3溶液时,测得生成沉淀和所加
入Na2CO3溶液的体积曲线关系如图所
示。若CaCl2的浓度为0.25mol/L,则
原溶液的pH为 ( )
A.0 B.1
C.2 D.3
Ⅱ卷(共 46 分)
26.已知HA的酸性比HB弱,在物质的量浓度均为0.1mol/L的NaA和NaB混合溶液中,下列排序正确的是 ( )
A.c(OH-) > c(HA) > c(HB) > c(H+)
B.c(OH-) > c(A-) > c(B-) > c(H+)
 C.c(OH-) > c(B-) > c(A-)
> c(H+)
C.c(OH-) > c(B-) > c(A-)
> c(H+)
D.c(OH-) > c(HB) > c(HA) > c(H+)
25.在一含Na+的澄清溶液中,可能还存在NH4+.Fe2+.I-.Br-.CO32-.SO32-六种离子中的几种:①在原来溶液中滴加足量的饱和氯水,有气泡生成,溶液呈现橙黄色
②向呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成
③橙黄色溶液不能使淀粉溶液变蓝色。
根据上述实验事实推断,下列说法不正确的是 ( )
A.溶液中一定存在Br-.CO32- B.溶液中可能存在NH4+
C.溶液中一定不存在Fe2+.I-.SO32- D.溶液一定呈碱性
24. 某稀溶液中含有Fe(NO3)3.Cu(NO3)2.HNO3,
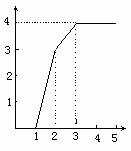
某稀溶液中含有Fe(NO3)3.Cu(NO3)2.HNO3,
向其中逐渐加入铁粉,溶液中Fe2+的浓度(纵
坐标)和加入铁粉的物质的量(横坐标)之间
的关系入右图所示,则溶液中Fe(NO3)3.
Cu(NO3)2.HNO3物质的量浓度之比为( )
A.1:1:1
B.1:3:1
C.3:3:8
D.1:1:4
23.设NA代表阿伏加德罗常数的数值,下列说法中正确的是 ( )
①常温常压下,17克甲基(-14CH3)所含的中子数为9NA
②常温常压下,22.4 LNO气体的分子数小于NA
③64克铜发生氧化还原反应,一定失去2NA个电子
④1molSiO2晶体中含有的Si-O共价键数目为4NA
⑤1molFeCl3跟水完全反应转化为为氢氧化铁胶体后,其中胶体粒子数目为NA
⑥常温常压下, 1mol氦气含有的核外电子数为4NA
A.①② B.③④ C.②④ D.⑤⑥
22.在一个固定体积的密闭容器中,保持一定温度,进行以下反应:H2(g)+I2(g) 2HI(g)。已知起始时加入1 mol H2和2 mol I2(g),当达到平衡时HI的体积分数为φ。下列四种情况分别投入上述容器,且始终保持原温度,平衡时HI的体积分数也为φ的是、( )
A.2 mol H2和1 mol I2(g) B.3 mol HI
C.2 mol H2和2 mol I2(g) D.1 mol I2(g)和2 mol HI(g)
21.在t1℃时反应2A(g) B(g)达到平衡,混合气体的平均相对分子质量为M1,t2℃时设反应平衡后混合气体的平均相对分子质量为M2,当温度从t1℃升高到t2℃时,下列说法正确的是 ( )
B(g)达到平衡,混合气体的平均相对分子质量为M1,t2℃时设反应平衡后混合气体的平均相对分子质量为M2,当温度从t1℃升高到t2℃时,下列说法正确的是 ( )
A.若M1>M2,平衡右移,正反应吸热
B.若M1<M2,平衡左移,正反应吸热
C.若M1>M2,平衡左移,正反应放热
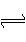 D.若M1<M2,平衡右移,正反应放热
D.若M1<M2,平衡右移,正反应放热
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com