
题目列表(包括答案和解析)
16.X、Y、Z、W四种元素在周期表中相对位置如图,Y、Z质子数之和为21,下列说法正确的是
|
|
X |
|
Y |
|
Z |
|
W |
|
A.常压下,四种元素单质中,W单质的熔点最高
B.X的气态氢化物比Y的气态氢化物稳定
C.Z的阳离子与Y的阴离子电子层结构相同
D.W元素的金属性比Z元素金属性强 17.往含0.2 mol NaOH和0.1 mol Ca(OH)2的溶液中持续稳定地通入CO2气体,当气体为6.72 L(标态)时立即停止,则这一过程中,溶液中离子的物质的量和通入CO2气体的体积关系正确的图象是(气体的溶解忽略不计)

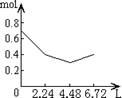

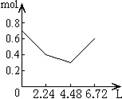
A B C D
15.现有A、B两种短周期元素,相同物质的量该两元素的单质与足量盐酸溶液反应产生气体体积比为2:3(同温、同压),如相同质量的该两元素单质与足量盐酸溶液反应产生体积比为2 :1(同温、同压)。A、B两元素分别为
A. Mg、Al B. Li、Mg C. Be、Al D.Be、Mg
14. 1mol过氧化钠与1mol碳酸氢铵固体混合后,在密闭的容器中加热充分反应,排出气体物质后冷却,残留的固体物质是
A.Na2CO3 B.Na2O2 Na2CO3
C.NaOH Na2CO3 D.Na2O2 NaOH Na2CO3
13.已知在热的碱性溶液中,NaClO发生如下反应:3NaClO=2NaCl+NaClO3。在相同条件下NaClO2也能发生类似的反应,其最终产物是( )
A.NaCl、NaClO B.NaCl、NaClO3
C.NaClO、NaClO3 D.NaClO3、NaClO4
12.在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,1molCuSO4能氧化磷的物质的量是
A.2/5 mol B.1/5 mol C.11/5 mol D.1/3 mol
11.已知14mol/L H2SO4溶液的溶质质量分数为80%,则7mol/L H2SO4溶液的溶质质量分数将
A.大于40% B.小于40% C.等于40% D.无法确定
10.下列实验过程能引起结果偏高的是
①配制100g10% CuSO4溶液,称取10g CuSO4晶体溶于90g水中
②测定CuSO4晶体中结晶水的百分含量时,所用的晶体已经受潮
③配制一定物质的量浓度的硫酸溶液时,定容时俯视容量瓶的刻度线
④质量分数为10%和90%的两种硫酸等质量混合配制50%的硫酸溶液。
⑤质量分数为30%和10%的两种氨水等体积混合配成20%的氨水。
A. ①⑤ B. ②④ C. ②③ D. ④⑤
9.下列分子中各元素原子最外层电子全部参与成键的是
A. HF B. CO2 C. CH4 D. Cl2
8.实验室保存下列试剂,其中保存方法和理由描述都正确的是
|
编号 |
试 剂 |
保存方法 |
理 由 |
|
A |
固体氢氧化钠 |
存放在带橡皮塞广口瓶中 |
防止空气接触被氧化,防止和水蒸气、二氧化碳接触而变质 |
|
B |
碳酸钠晶体 |
存放在干燥密封广口瓶中 |
防止风化成粉末而变质 |
|
C |
液溴 |
存放在带橡皮塞细口瓶中 |
防止挥发 |
|
D |
硝酸银溶液 |
存放在无色玻璃塞试剂瓶 中,放在冷暗处 |
防止见光分解 |
7.下列离子方程式正确的是
A.过氧化钠固体与水反应 2O22-+2H2O=4OH-+O2↑
B.在H2O2中加入酸性KMnO4溶液 2MnO4-+5H2O2+6H+=2Mn2+ +5O2↑+8H2O
C.NaHSO4溶液中滴入Ba(OH)2溶液至中性 H++SO42-+Ba2++OH-=BaSO4↓+H2O
D.次氯酸钙溶液中通入过量二氧化碳
Ca2++2ClO-+H2O+CO2 = CaCO3↓+2HClO
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com