
题目列表(包括答案和解析)
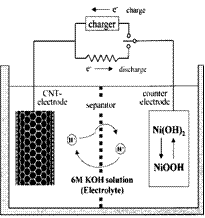
11.一种碳纳米管(氢气)二次电池原理如右图,该电池的电解质为6mol/LKOH溶液,下列说法不正确的是
A.储存H2的碳纳米管作电池正极
B.放电时负极附近pH减小
C.放电时电池正极的电极反应为:
NiO(OH)+H2O+e-=Ni(OH)2 +OH-
D.放电时,电池反应为2H2+O2=2H2O
10.设NA表示阿伏加德罗常数的数值,下列说法中不正确的是
 A.一定量的Fe与1 mol HNO3的稀硝酸恰好反应,则被还原的氮原子数小于NA
A.一定量的Fe与1 mol HNO3的稀硝酸恰好反应,则被还原的氮原子数小于NA
 B.160 g CuO 加热到1273K时完全分解,若转移2NA个电子,则反应方程式为:2CuO 2Cu+O2↑
B.160 g CuO 加热到1273K时完全分解,若转移2NA个电子,则反应方程式为:2CuO 2Cu+O2↑
 C.N60结构如右图,28 g N60单质中含有的N-N键个数为NA
C.N60结构如右图,28 g N60单质中含有的N-N键个数为NA
D.0.6 g CaCO3与Mg3N2的混合物中所含质子数为0.3NA
9.乙醇、液氨、水都可以发生自偶电离,如H2O + H2O H3O+ + OH-,
H3O+ + OH-,
NH3+NH3  NH4++ NH2-,则下列叙述正确的是
NH4++ NH2-,则下列叙述正确的是
A.乙醇的电离方程式:2CH3CH2OH  CH3CH2OH2+
+ CH3CH2O-
CH3CH2OH2+
+ CH3CH2O-
B.液氨的离子积常数为:1.0×10-28,则液氨浓度为1.0×10-14mol/L
C.若可用与pH相当的定义来规定pOH、pNH2-等,则乙醇中与pH相当的为-lgc(CH3CH2OH2+)
D.乙醇中KW = c(CH3CH2OH2+).c(CH3CH2O-)= 1.0 × 10-30,则此时的p CH3CH2O-=-15
8. 常温下,有甲、乙两份体积均为l L,浓度均为0.1mol/L的氨水,其pH为11。①甲
用蒸馏水稀释100倍后,溶液的pH将为a;②乙与等体积、浓度为0.2mol/L的盐酸
混合,在混合溶液中:n(NH4+)+n(H+)-n(OH-)=bmol。则a、b正确的答案组合是
A.9-11之间; 0.1 B.9-11之间; 0.2
C.12-13之间; 0.2 D.13; 0.1
7.不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,一定能产生沉淀的组合是
|
序号 |
甲 |
乙 |
丙 |
|
① |
CO2 |
SO2 |
石灰水 |
|
② |
HCl |
CO2 |
石灰水 |
|
③ |
CO2 |
SO2 |
Ba(NO3)2 |
|
④ |
NO2 |
SO2 |
BaCl2 |
|
⑤ |
CO2 |
NH3 |
CaCl2 |
A.②③④ B.②③④⑤ C.①③④ D.①②③④
6.在c(H+)∶c(OH-)=1∶2的水溶液中能大量共存的离子组是
A.K+、Al3+、H2PO4-、SO42- B.Ca2+、NH4+、CO32-、Cl-
C.Na+、K+、NO3-、ClO- D.Na+、Ba2+、I-、SO32-
5.下列离子方程式正确的是
A.60 mL1mol/L 氢氧化钡溶液与15mL2 mol/L 明矾溶液混合:
3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓
B.60 mL1 mol/L纯碱溶液与20 mL2 mol/L胆矾溶液混合(无气体放出):
3CO32-+2Cu2++2H2O=2HCO3-+Cu2(OH)2CO3↓
C.H2O中投入Na218O2固体:2H2O+218O22-=418OH-+O2↑
D.0.1mol/L CuCl2溶液中加入0.1mol/L NaHS溶液Cu2++2HS-+2H2O=Cu(OH)2↓+2H2S↑
4. 常温常压下,在带有相同质量活塞的容积相等的
常温常压下,在带有相同质量活塞的容积相等的
甲、乙两容器里,分别充有二氧化氮和空气,现
分别进行下列两实验:(N2O4 2NO2 △H >0)
2NO2 △H >0)
(a)将两容器置于沸水中加热
(b)在活塞上都加2 kg的砝码
在以上两情况下,甲和乙容器的体积大小的比较,
正确的是
A.(a)甲>乙,(b)甲>乙 B.(a)甲>乙,(b)甲=乙
C.(a)甲<乙,(b)甲>乙 D.(a)甲>乙,(b)甲<乙
3.下列叙述中,错误的是
A.虽然固体氯化钠不能导电,但氯化钠是电解质
B.纯水的pH随温度的升高而减小
C.在醋酸钠溶液中加入少量氢氧化钠,溶液中c(OH-)增大
D.在纯水中加入少量硫酸铵,可抑制水的电离
2.某炼金厂的废水因暴雨溢出,导致河水严重污染。废水中所含CN-有剧毒,其性质与卤素离子相似,还原性介于I-与Br-之间,HCN为弱酸。下列说法不正确的是
A.CN-可以和稀硫酸反应生成HCN B.CN-可被Cl2氧化成(CN)2
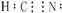 C.在水溶液中(CN)2可被F-还原 D.HCN的电子式为
C.在水溶液中(CN)2可被F-还原 D.HCN的电子式为
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com