
题目列表(包括答案和解析)
16. 某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)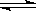 2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的
2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的
量),根据如图可得出的判断结论正确的是
A.反应速率a>b>c
B.达到平衡时A2的转化率大小为:b>a>c
C.若T2>T1,则正反应一定是放热反应
D.b点时,平衡体系中A、B原子数之比接近1∶3
15.某二元酸(化学式H2A)在水中的电离方程式是:H2A
= H+ + HA-,HA- H++A2-,又知0.1mol·L-1NaHA溶液的pH
= 2。则下列说法不正确的是
H++A2-,又知0.1mol·L-1NaHA溶液的pH
= 2。则下列说法不正确的是
A.因为A2-+H2O  HA-+OH-,所以Na2A溶液显碱性
HA-+OH-,所以Na2A溶液显碱性
B.0.1mol·L-1 H2A溶液中氢离子的物质的量浓度为0.11 mol·L-1
C.NaHA溶液中各种离子浓度的关系是c(Na+ ) > c(HA-) > c(H+) > c(A2-) > c(OH- )
D.在NaHA溶液中,HA-电离的趋势大于其水解的趋势
14.今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,分别取三份各100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是
A.100mL溶液中含0.01mol CO32- B.Cl-一定存在
C.K+一定存在 D. Ba2+一定不存在,Mg2+可能存在
13.甲、乙两杯醋酸稀溶液甲的pH=a,乙的pH=a+1,对下列叙述的判断正确的是
①甲由水电离出来的H+的物质的量浓度是乙的1/10倍
②物质的量浓度c(甲)=10c(乙)
③中和等物质的量的NaOH溶液需甲、乙两杯酸的体积,10V(甲)>V(乙)
④甲中的c(OH-)为乙中的c(OH-)的10倍
A.①②④正确 B.①③正确 C.②④正确 D.只有①正确
12.珍爱生命,远离毒品。以下是四种毒品的结构简式,下列有关说法正确的是
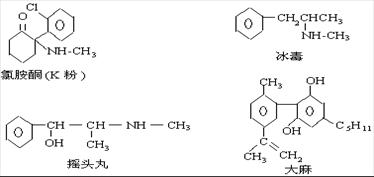
A.这四种毒品都属于芳香烃
B.摇头丸不可能发生加成反应
C.1mol大麻最多可与含4mol Br2 的浓溴水发生反应
D.K粉的分子式为C13H16ClNO
|
11.短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍。下列说法正确的是
A.X的氢化物溶于水显酸性
B.Y的氧化物是离子化合物
C.Z的氢化物的水溶液在空气中存放不易变质
D.X和Z的最高价氧化物对应的水化物都是弱酸
10. 阿伏加德罗常数约为6.02×1023mol-1,下列说法一定正确的是
阿伏加德罗常数约为6.02×1023mol-1,下列说法一定正确的是
A.60g SiO2晶体中,含有2×6.02×1023个Si-O键
B.标准状况下,2.24LCHCl3含有的分子数为0.1×6.02×1023
C.720g C60晶体含有6.02×1023个如图中晶胞单元
D.7.8g Na2O2中含有的离子总数为0.3×6.02×1023
9.下列反应的离子方程式正确的是
A. 过量的NaHSO4与Ba(OH)2溶液反应: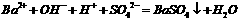
B.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2
C. AgNO3溶液中加入过量的氨水:Ag++NH3·H2O=AgOH +NH4+
D.氢氧化铝中和胃酸:Al(OH)3+3H+=Al3++3H2O
8.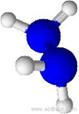 肼(N2H4)是航天飞船常用的高能燃料,肼(N2H4)分子中所示原子均达到稀有气体原子的稳定结构,它的沸点高达l13℃,燃烧热为642 kJ·mol-1,肼与氧气及氢氧化钾溶液还可构成燃料电池。已知肼的球棍模型如右图所示,下列有关说法正确的是
肼(N2H4)是航天飞船常用的高能燃料,肼(N2H4)分子中所示原子均达到稀有气体原子的稳定结构,它的沸点高达l13℃,燃烧热为642 kJ·mol-1,肼与氧气及氢氧化钾溶液还可构成燃料电池。已知肼的球棍模型如右图所示,下列有关说法正确的是
A.肼是由极性键和非极性键构成的非极性分子
B.肼沸点高达l13℃,可推测肼分子间可形成氢键
C.肼燃烧的热化学方程式为: N2H4(g)+O2(g) = N2(g) +2H2O(g);△H=-642 kJ·mol-1
D.肼-氧气燃料电池,负极的电极反应为:O2 +2H2O+4e-=4OH-
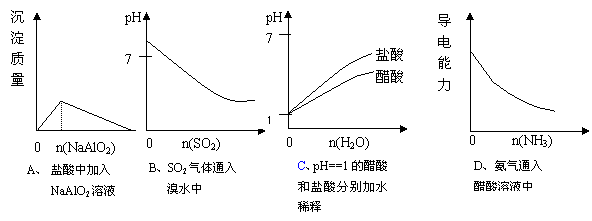
7.下列实验过程中产生的现象与对应的图形正确的是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com