
题目列表(包括答案和解析)
1.下列有关实验操作错误的是 ( )
A.用药匙取用粉末状或小颗粒状固体 B.用胶头滴管滴加少量液体
C.给盛有2/3体积液体的试管加热 D.倾倒液体时试剂瓶标签面向手心
27.(8分)为了测定Cu、Ag合金的成分,将20.0g合金溶于80mL13.5mol·L-1的浓度 HNO3中,待合金完全溶解后,收集到标准状况下6.72L气体,并测得溶液中c(H+)=1 mol·L-1。若反应后溶液体积仍为80mL。试计算:
(1)被还原的HNO3的物质的量为 ;
(2)判断产物中气体的成分(填化学式)及体积。
26.(7分)A、B、C、D、E五种可溶性化合物,分别由阳离子Fe3+、Ba2+、Al3+、Na+、Ag+和阴离子NO3-、OH-、SO42-、Cl-、CO32-中的各一组成(离子不重复)。现做如下实验:
①A和E的溶液显碱性,0.1mol/LA溶液的pH小于13;
②在B的溶液中逐滴加入氨水有白色沉淀生成,继续加氨水至过量,沉淀消失;
③在C的溶液中加入铁粉,溶液的质量增加;
④在D的溶液中加入过量的Ba(OH)2溶液,没有沉淀。
(1)根据以上事实推断A、B、E的化学式:
A 、B 、E
(2)写出③和④的离子方程式:
③
④
25.(10分)
(1)下面是用98%的浓度H2SO4(ρ=1.84/cm3)配制成0.5mol·L-1的稀H2SO4500mL的操作,请按要求填空:
①所需浓H2SO4的体积为
②如果实验室有15mL、20mL、50 mL量筒,应选用 mL,量筒最好。
③将量取的浓H2SO4沿烧杯内壁慢慢注入盛有约100 mL水的烧杯里,并不断搅拦,目的是 。
④将 的上述溶液沿 注入中,并用50 mL蒸馏水洗涤烧杯2-3次,洗涤液要一并注入上述容器中,并摇匀。
⑤加水至距刻度1-2㎝时,改用 加水,使溶液的凹液面正好跟刻度相平。
(2)某同学在配制NaOH溶液时有以下现象发生,则对所配溶液的物质的量浓度有何影响?(填偏高、偏低或不变)
①定容时观察液面俯视 ;
②NaOH颗粒表面部分变质 ;
③用胶头滴管向容量瓶中加水时凹面高于刻度线,此时立即用胶头滴管将瓶内液体吸出,使凹液面与刻度线相切 。
24.(6分)某同学要做检验Na2CO3粉末中含有少量的NaOH和NaCl的实验。他的实验设计分为七个步骤,其中的5个步骤所用的试剂及实验操作均已写明,见下表:
|
实验步骤 |
所用实验试剂及操作 |
|
( ) |
取少量样品放入试管甲中 |
|
( ) |
再向溶液里滴加几滴AgNO3溶液 |
|
( ) |
过滤,取少量滤液盛在试管乙里 |
|
( ) |
向试管加入适量的蒸馏水,振荡 |
|
( ) |
滴加几滴酚酞试剂 |
|
( ) |
|
|
( ) |
|
试将上表里尚缺的两个步骤所用的试剂(自选)及实验操作补写完整,然后按实验步骤的顺序以①、②、③、④、⑤、⑥、⑦分别填入相应的“实验步骤”栏里。
23.(6分)CO和CO2的混合气体18g,完全反应后测得CO2体积为11.2L(标准状况)。试回答:
(1)混合气体中CO的质量是 。
(2)混合气体中CO2在标准状况下的体积是 。
(3)混合气体在标准状况下的密度是 。
 21.(8)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如:
21.(8)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如:
(1)在上述有编号的步骤中,需用还原剂的是 ,需用氧化剂的是 。
(2)在上述循环中,既能与强酸反应又能与强碱反应的两性物质是 (填化学式)
(3)完成并配平步骤①的化学方程式,标出电子转移的方向和数目:
□Na2Cr2O7+□KI+□HCl→□CrCl3+□NaCl+□KCl+□I2+□
22.(5分)写出下列反应的离子方程式:
(1)用烧碱溶液吸收氯气 ;
(2)铜与氯化铁溶液反应 ;
(3)铝与氢氧化钠反应 ;
(4)澄清石灰水中通入少量二氧化碳 ;
(5)碳酸钠溶液显碱性的原因 。
19.在下表中,欲用一种试剂Z来判别盐溶液中的离子X和离子Y是否存在时,此试剂使用正确的是 ( )
|
试剂Z |
离子X |
离子Y |
|
A.氨水 |
Al3+ |
Mg2+ |
|
B.硝酸银 |
Cl- |
CO32- |
|
C.硫酸钠 |
Ba2+ |
Ca2+ |
|
D.硝酸钠 |
SO42- |
Cl- |
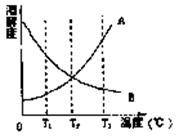 20.右图是A、B两物质的溶解度随温度变化的曲线图,A、B均不是与水反应的物质,在T3℃时,将A、B两物质分别溶于100g水中,刚好配成饱和溶液,然后降温,试根据曲线判断下列A与B的比较中正确的是 ( )
20.右图是A、B两物质的溶解度随温度变化的曲线图,A、B均不是与水反应的物质,在T3℃时,将A、B两物质分别溶于100g水中,刚好配成饱和溶液,然后降温,试根据曲线判断下列A与B的比较中正确的是 ( )
A.T3℃时,A的溶解度比B大
B.T2℃时时,A、B两物质所形成的溶液里溶质的质量分数
相等
C.T1℃时,A形成的溶液的溶质的质量分数较小
D.T3℃降到T1℃时,A、B两物质所形成的溶液的质量均不变
|
18.有X2、Y2、Z2三种非金属单质,它们的有关反应有:(a)2X-+Z2→2Z-+X2,(b)2 Z-+Y2→2Y-+Z2,下列关于它们的叙述中不正确的是 ( )
A.氧化 性Y2>Z2>X2 B.W2的还原性比Z2弱
C.W2与Y-能发生反应 D.W2与Y-不能发生反应
17.下列离子方程式中正确的是 ( )
A.澄清石灰水与稀盐酸反应:Ca(OH)2+2H+==Ca2+2H2O
B.钠与水的反应:Na+2H2O==Na++2OH-+H2↑
C.铜片插入硝酸银溶液中:Cu+Ag+==Cu2+Ag
D.大理石溶于醋酸的反应:CaCO3+2CH3COOH==Ca2+2CH3COO-+CO2↑+H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com