
题目列表(包括答案和解析)
21.(16分)、饮用水质量是关系人类健康的重要问题。
(1)氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为__________________________________,所生成的次氯酸的电子式为:____________。
(2)写出工业上制取漂白粉的化学反应方程式:
______________________________________。
(3)ClO 2被称为“第四代”饮用水杀虫剂,因其高效率,无污染而被广泛使用.制备ClO 2是发达国家普遍重视的课题,我国北京永利科技有限公司已用电解法批量生产ClO 2。
其反应原理为:4ClO 3-+4H+=4 ClO 2+O 2↑+2H 2O 试写出两电极反应式:
阴极:_______________________________________________________
阳极:_______________________________________________________
(4)相同物质的量的氯气与二氧化氯消毒时转移电子数目之比是__________________
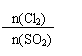 (5)采用氧的一种同素异形体用于自来水消毒,既提高了消毒效率,安全无副作用,该物质在自然界中存在,对地球生命体起保护伞作用。该物质和氯气溶于水以及SO2的漂白原理分别是____________________,____________________,__________________;若将氯气与SO2二者混合,若想使石蕊试液褪色则
范围为__________________。
(5)采用氧的一种同素异形体用于自来水消毒,既提高了消毒效率,安全无副作用,该物质在自然界中存在,对地球生命体起保护伞作用。该物质和氯气溶于水以及SO2的漂白原理分别是____________________,____________________,__________________;若将氯气与SO2二者混合,若想使石蕊试液褪色则
范围为__________________。
20.标准状况下,将CO2和CO混合气体(密度为1.79g/L)充满一盛有足量Na2O2的密闭容器(体积为22.4L,固体体积可忽略不计)用不间断的电火花引发至充分反应,下列对完全反应后容器里残留物的叙述正确的是 ( )
A.有0.125molO2 B.有0.375molO2
C.有0. 5molCO D.有0.25molNa2CO3
19.氢气、氧气、氯气按体积比9:4:1混合,在一定条件下充分反应,冷却后所得溶液的质量分数为 ( )
A.36.5% B.33.6% C.30.3% D.20.2%
18.在相同条件下,有4支试管盛有等体积混合的4种混合气体,它们分别是 ①NO2和NO②NO2和O2③NH3和N2④H2和NO,现将4支试管均倒扣于水中,充分反应后,水面上升高度依次为a、b、c、d其关系正确的是 ( )
A.a=b=c=d B.c>b>a>d C.b>c>a>d D.a>b>c>d
17.硫磺在空气中燃烧生成气体甲,甲溶于水得溶液乙,向乙溶液中滴加溴水,溴水褪色乙变成丙。在丙里加入Na2S生成气体丁,把丁通入乙得到沉淀戊。甲、乙、丙、丁、戊均含有硫元素,则们正确的顺序是 ( )
A.SO3 、H2SO4 、H2SO3 、H2S 、S
B.SO2 、H2SO3 、H2SO4 、SO2 、SO3
C.SO3 、H2SO4 、H2SO3 、SO2 、Na2S2O3
D.SO2 、H2SO3 、H2SO4 、H2S 、S
16.下列物质反应时,生成物只有一种的是 ( )
A.镁在空气中燃烧 B.镁在二氧化碳中燃烧
C.磷在氯气中燃烧 D.氢气在氯气中燃烧
15.对下列物质 ①氢硫酸 ②亚硫酸钠溶液 ③氯水 ④硫酸亚铁溶液 ⑤氢氧化钠溶液,只需观察试剂瓶内的情况就可作出该试剂是否变质结论的是 ( )
A.①②③ B.①②⑤ C.①③④ D.①②③④⑤
14.欲将混合液中Al3+、Cu2+、Ba2+、Ag+逐一沉淀出来加以分离,加入试剂 ①Cl- ②SO42- ③OH- ④CO2⑤CO32-的正确顺序是 ( )
A.①②③④ B.③⑤①② C.②①③⑤ D.①⑤③②
13.在500mL 1mol/L FeCl3溶液中加入铁粉,反应完全后,滤去多余铁粉,在滤液中加入足量的NaOH溶液,所得沉淀的物质的量是 ( )
A.0.5mol B.0.75mol C.1mol D.1.5mol
12.下列各组离子中,在溶液中能大量共存,加入强碱有沉淀生成,加入强酸能放出气体的是 ( )
A.Mg2+ Cl- HCO3- SO42- B.Na+ Ca2+ NO3- HPO42-
C.NH4+ Cu2+ Cl- SO42- D.NH4+ K+ Cl- CO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com