
题目列表(包括答案和解析)
6.为了使鱼苗顺利运输,必须满足三个条件:①需要保持体积适量的氧气,②使鱼苗呼出的二氧化碳及时排除,③防止细菌大量繁殖,已知下述四种物质加入水中都可以起到供氧杀菌作用,在长距离储运鱼苗的水中,最好加入的药剂是 ( )
A.Na2O2 B.Cl2 C.CaO2·2H2O D.H2O2
5.不能用H++OH-==H2O表示的离子反应的是 ( )
A.氢氧化钠溶液和硫酸氢钠溶液 B.氢氧化钡和硫酸溶液
C.硫酸氢铵溶液和少量氢氧化钠溶液 D.石灰水和硝酸溶液
4.某溶液中含有HCO3-、SO32-、S2-、ClO-等4种阴离子。若向其中少量的 Na2O2后,溶液中离子浓度基本保持不变的是 ( )
A.ClO- B.SO32- C.S2- D.HCO3-
3.已知(1)HCl和NaOH反应的中和热ΔH=-57.3kJ/mol;
(2)CO(g)的燃烧热是283.0kJ/mol;则下列描述正确的是 ( )
A.H2SO4和NaOH反应的中和热ΔH=2×(-57.3)kJ/mol
B.2CO2(g) =2CO(g)+O2(g);ΔH=+2×283.0kJ/mol
C.1/2H2SO4(浓)+NaOH(aq)=1/2Na2SO4(aq)+H2O(1); △H=-57.3kJ/mol
D.1mol甲烷燃烧所放出的热量是甲烷的燃烧热
2.下列有关氧化还原反应的叙述中正确的是 ( )
A.有单质参加或有单质生成的反应一定是氧化还原反应
B.氧化还原反应的本质是元素化合价的升降
C.金属单质在化学反应中一定作还原剂
D.失电子的反应物在反应中作还原剂,生成还原产物
1.下列试剂的浓溶液在空气中久置都会变质,在变质过程中只发生了氧化还原反应的是
( )
A.钠 B.过氧化钠 C.次氯酸钙 D.过氧化氢[i]
25.(6分)、把2.24g铁和100mL稀HNO3溶液混合后充分反应,铁和HNO3均无剩余,向反应后的溶液中加入50mL 0.2mol·L-1的KI溶液,恰好使溶液中的Fe3+全部还原为Fe2+。求原稀HNO3 的物质的量浓度?
24.(5分)、镁、铝、硅的混合物25g,跟足量盐酸反应生成氢气22.4L(标况),另取同样质量的此混合物跟足量烧碱溶液反应,产生氢气仅为前者的一半,试计算原混合物中镁、铝、硅质量各为多少g?
23.(19分)、资料显示:“氨气可在纯氧中安静燃烧……”。某校化学小组学生设计如下装置
(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。
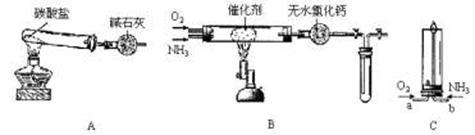
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是________;碱石灰的作用是________。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式是___________________________________________;
试管内气体变为红棕色,该反应的化学方程式是_____________________________。
②停止反应后,立即关闭B中两个活塞。一段时间后,将试管浸入冰水中,试管内气体颜色变浅,请结合化学方程式说明原因_________________________________。
(3)将过量的氧气与A产生的氨气分别从A.b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的先后顺序是___________________,其理由是A.
______________________________B._________________________。
②氨气燃烧的化学方程式是_______________________________________________。
22.(14分)、A-N均为中学化学中的常见物质,其中A是日常生活中不可缺少的物质,也是化工生产上的重要原料,单质M是目前使用量最大的金属,常温下B、E、F为气体,G为无色液体,这些物质在一定条件下存在如下转化关系,其中有些反应物或生成物已经略去。回答下列问题:

(1)H的化学式为 ,D的电子式为 。
(2)K转变为I的离子方程式: 。
(3)D与G反应的化学方程式为 。
(4)I可用于净水,其原因是
(用相关的反应方程式和简要文字回答)。
(5)1mol气体E在气体F中完全燃烧生成液态G时放出的热量为a kJ,请写出表示E燃烧热的热化学方程式 。
(6)I与NaClO在碱性条件下反应,是制备理想的绿色水处理剂(Na2MO4)的一种方法,试写出此反应的化学方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com