
题目列表(包括答案和解析)
22.(4分)工业上常用漂白粉跟酸反应制得的氯气对漂白粉的质量分数(x%)来表示漂白粉的优劣。现为测定一瓶漂白粉的x%,进行如下实验:称取漂白粉样品2.00g,加水研磨后转入250mL容量瓶内,用水稀释至刻度。摇匀后,取出25.0mL,加入过量的KI溶液和过量的稀硫酸,静置待漂白粉放出的氯气与KI完全反应后,加入0.100mol·L-1的Na2S2O3溶液20.00mL,恰好与生成的碘完全反应:
2Na2S2O3+I2=Na2S4O6+2NaI
(1)试写出漂白粉与稀硫酸反应的化学方程式 。
(2)试由上述数据计算该漂白粉的x%为 。
21.(8分)某溶液由Na+、Cu2+、Ba2+、Fe3+、AlO2-、CO32-、SO42-、Cl-中的若干种离子组成,取适量该溶液进行如下实验:
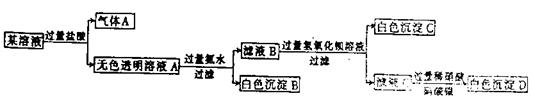
根据上述实验回答下列问题:
(1)气体A的化学式是 ,白色沉淀B的摩尔质量是 。
(2)生成沉淀C的离子方程式是 。
(3)原溶液中一定不存在的离子是 。
19.(10分)(1)配平氧化还原反应方程式:
C2O42-+ MnO4-+ H+= CO2+ Mn2++ H2O
(2)称取6.0g含H2C2O4·2H2O、KOH、KHC2O4和K2SO4的试样,加水溶解,配成250mL溶。量取两份此溶液各25mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25mol/LNaOH溶液至20mL时,溶液由无色变为浅红色。该溶液被中和的H+的物质的量为 mol。
②第二份溶液中滴加0.10 mol/L的酸性高锰酸钾溶液至16mL时反应完全,此时溶液颜色 。该溶液中还原剂的物质的量为 mol。
③原试样中H2C2O4·2H2O的质量分数为 。
 20.(14分)某校学生课外活动小组为测定Na元素的相对原子
20.(14分)某校学生课外活动小组为测定Na元素的相对原子
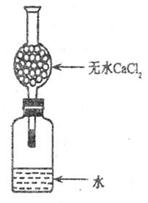
质量,设计的装置如右图,从实验室取出bg(不足量)的
钠放入水中,塞紧瓶塞,使钠完全反应,试回答:
(1)实验室取用一小块钠,需要的用品有 。
(2)此干燥管的作用是 ,若不用些干燥管,
则测出相对原子质量会比实际相对原子质量
(填“偏大”、“偏小”或“不变”,下同),若此钠
块有极少量被氧化,则结果会 。
(3)有甲同学建议在图中干燥管上再第二个干燥管(设此
干燥质量为mg,包括干燥刘的质量),其目的是 ,
称得反应前装置(包括水和干燥剂)的总质量为ag。完
全反应后再称量此装置的总质量为cg,且第二个干燥管质量变为m1g,则依甲同学建议,计算钠的相对原子质量的表达式为 。
(4)有乙同学为避免由于行动不够迅速产生偏差,又建议在广口瓶中再加入一定量煤油,其目的是 。
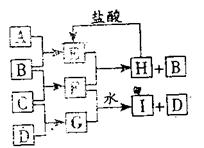
的成分。F的焰色反应呈黄色。在G中,非金属
元素与金属元素的原子个数比为1:2。在一定条
件下,各物质之间的相互转化关系如右图所示
(图中部分产物未列出):
请填写下列空白
(1)A是 ,G的电子式 。
(2)H与盐酸反应生成E的离子方程式是 。
(3)E与F反应的化学方程式是 。
(4)F与G的水溶液反应生成I和D的离子方程式是 。
18.(6分)已知固体混合物A由NaHCO3,KHCO3,MgCO3,CaCO3四种物质中的两种混合而成。取A与足量的盐酸反应,请通过计算和推理回答下列问题:
(1)若n(A)为定值,生成气体的量即为定值,则A的组成可能有 种。
(2)若m(A)为定值,生成气体的量即为定值,则A的可能组成是
(填写化学式)。
17.(10分)A、B、C、D是按原子序数由小到大排列
16.2LN2和CH4的混合气体与4LO2点燃充分反应后,用干燥剂除去水分,剩余气体的体积5L。原来混合气体中N2和CH4的物质的量之比(各气体体积都在相同的温度、压强下测定)为 ( )
A.1:3 B.1:1 C.2:1 D.3:1
第Ⅱ卷(非选择题 共52分)
 二、填空题(共52分)
二、填空题(共52分)
15.下列叙述中指定粒子的数目大于6.02×1023的是 ( )
A.2g重水(D2O)中含有的中子数
B.0.1 mol F-中含有的电子数
C.标准状况下,11.25LN2和NO混合气体中的原子数
D.1L1 mol/Lna2SO4溶液中的Na+数
14.在反应3BrF3+5H2O=HB rO3+Br2+9HF+O2↑中,若有5molH2O参加反应,则被水还原的BrF3的物质的量为 ( )
A.3mol B.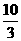 mol C.
mol C. mol D.2 mol
mol D.2 mol
13.中学化学教材中有大量数据,下列为某同学对数据的利用情况,其中不正确的是( )
A.用反应物、产物中键能数据可判断对应反应的热效应
B.用沸点数据推测将一些液体混合物用分镏的方法分离开来的可能性
C.有反应热数据的大小判断不同反应的反应速率的快慢
D.用原子(或离子)半径数据推断某些原子(或离子)氧化性或还原性的强弱
12.在一定温度下,向饱和的烧碱溶液中加入一定量的Na2O2,充分反应后,恢复到原来的温度,下列说法中正确的是 ( )
A.溶液的pH不变,有H2放出
B.溶液的pH值增大,有O2放出
C.溶液中c(Na+)增大,有O2放出
D.溶液中Na+数目减少,有O2放出
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com