
题目列表(包括答案和解析)
17.电解100mL含c(H+)=0.30mol/L的下列溶液,当电路中通过0.04mol电子时,理论上析出金属质量最大的是 ( )
A.0.10mol/LAg+ B.0.02mol/LZn2+
C.0.20mol/LCu2+ D.0.20mol/LFe3+
16.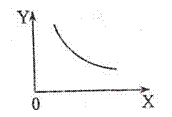 在一定条件下固定容积的密闭容器中,反应2NO2(g)
在一定条件下固定容积的密闭容器中,反应2NO2(g) O2(g)+2NO(g);△H>0达到平衡。当改变其中一个条件X,Y随X的
变化符合图中曲线的是 ( )
A.当X表示温度时,Y表示NO2的物质的量
B.当X表示压强时,Y表示NO2的浓度
C.当X表示反应时间时,Y表示混合气体的密度
D.当X表示起始时NO2的物质的量时,Y表
示平衡时O2的物质的量
15.下列溶液中,各组离子一定能够大量共存的是 ( )
A.使酚酞试液变红的溶液:Na+、C1-、SO42-、Fe3+
B.使甲基橙试液变红的溶液:Fe2+、Mg2+、NO3-、C1-
C.c(H+)=1.0×10-13mol/L的溶液中:Na+、S2-、SO32-、SO42-
D.含有大量A1O2-的溶液:K+、Ba2+、C1-、A13+
14.下列溶液中有关物质的量浓度关系正确的是 ( )
A.25℃时pH=2的HA溶液与pH=12的MOH溶液任意比混合:
c(H+)+c(M+)=c(OH-)+c(A-)
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液
c(NaOH)<c(CH3COONa)<c(Na2CO3)
C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-)+c(OH-)=c(H+)+c(CH3COOH)
D.0.1mol/L 的NaHA溶液,其pH=4
c(HA-)>c(H+)>c(H2A)>c(A2-)
13.常温下,用等浓度的盐酸分别中和等体积的0.01mol/L的Ba(OH)2、PH=12的NaOH和pH=12的NH3·H2O三种碱溶液,用去盐酸的体积分别为V1、V2、V3,则三者的大小关系正确的是 ( )
A.V3=V2=V1 B.V3>V1=V2
C.V1=V2>V3 D.V3>V1>V2
12.将1molSO2和1molO2通入恒温容密闭容器中,一定条件下达到平衡时SO3的物质的量为0.3mol,此时若移走0.5molSO2和0.5molO2,反应达到新的平衡时,SO3的物质的量是 ( )
A.0.15mol B.大于0.15mol
C.小于0.15mol D.大于,0.15mol,小于0.3mol
11.常温下,取物质的量浓度相等的NaOH溶液和HC1溶液,以2:1体积比相混合,所得溶液的pH等于12,则原溶液的物质的量浓度为 ( )
A.0.01mol/L B.0.02mol/L C.0.03mol/L D.0.04mol/L
10.下列有关金属腐蚀与防护的说法正确的是 ( )
A.纯银器表面在空气中渐渐变暗发生的是电化学腐蚀
B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C.在海轮外壳连接锌块可保护海轮外壳不受腐蚀
D.将地下输油管与外加直流电源的正极相连以保护它不受腐蚀
9.下列方程式中,属于水解反应的是 ( )
A.HCOOH+H2O
HCOO-+H2O+
B.CO2+H2O HCO3-+H+
C.HS-+H2O
S2-+H3O+
D.CO32-+H2O HCO3-+OH-
8.常温下,某溶液中由水电离的c(H+)=1×10-12mol/L,该溶液可能是 ( )
①二氧化硫水溶液 ②氯化铵水溶液
③硝酸钠水溶液 ④氢氧化钠水溶液
A.①② B.①④ C.②③ D.③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com